
Wetenschap
Formulegewicht versus molaire massa:de relatie begrijpen
* Formulegewicht is de som van de atoomgewichten van alle atomen in een chemische formule, uitgedrukt in atomaire massa-eenheden (amu) .
* Molar massa is de massa van één mol van een stof, uitgedrukt in gram per mol (g/mol) .
Dit is de belangrijkste verbinding:
* 1 amu is gelijk aan 1 g/mol.
Daarom:
* De numerieke waarde van de formule gewicht en molmassa is identiek.
*Het verschil zit alleen in de gebruikte eenheden.
Voorbeeld:
* De formule gewicht van water (H₂O) is 18 amu (1 + 1 + 16 =18).
*De molaire massa van water is 18 g/mol.
U kunt de termen formulegewicht en molmassa dus door elkaar gebruiken, zolang u maar weet welke eenheden worden gebruikt.
 Giftige, voor altijd chemicaliën gevonden in kraanwater roepen vragen op voor wetenschappers
Giftige, voor altijd chemicaliën gevonden in kraanwater roepen vragen op voor wetenschappers Landbouwhulpmiddelen in het oude Egypte
Landbouwhulpmiddelen in het oude Egypte  Wat is een goed zelfstandig naamwoord van boom?
Wat is een goed zelfstandig naamwoord van boom?  Deze plant zuigt! (Maar hoe?)
Deze plant zuigt! (Maar hoe?)  Arctische stoofpot:begrijpen hoe meren op hoge breedtegraden reageren op en invloed hebben op de klimaatverandering
Arctische stoofpot:begrijpen hoe meren op hoge breedtegraden reageren op en invloed hebben op de klimaatverandering
Hoofdlijnen
- Waarom zijn overervingspatronen bij mensen net zo gemakkelijk bestudeerde erwten of fruitvliegen?
- Hoe cellen hun afvalverwerkingssystemen opnieuw gebruiken om ontstekingen te bevorderen
- Hoe verschilt een prokaryote cel van eukaryote cellen?
- Wie ontdekte het eten van vleesbacteriën?
- Inzicht in splitsingsvoren:cytokinese in dierlijke cellen
- Waar zijn de sporten van DNA -laatste van gemaakt?
- Wat zijn de gemeenschappelijke hulpmiddelen die in de biologie worden gebruikt?
- Wat is Conservation Genetics?
- Wat is een onontwikkeld organisme?
- Snellere en goedkopere ethanol naar vliegtuigbrandstof in het verschiet

- Hydrogenering zonder waterstof:efficiënte katalyse in een stabiele emulsiegel
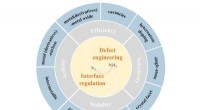
- Defect- en interface-engineering voor e-NRR onder omgevingsomstandigheden
- Onderzoekers kunnen gaatjes aanpassen in nieuw poreus materiaal

- Ontwerpen van biologische beweging op nanometerschaal

 Hoeveel energie is er in kantine -voedingsmiddelen?
Hoeveel energie is er in kantine -voedingsmiddelen?  Hoe huilen werkt
Hoe huilen werkt  Wetenschappers ontslagen van EPA Forge Ahead met onofficieel rapport over verontreinigende stoffen
Wetenschappers ontslagen van EPA Forge Ahead met onofficieel rapport over verontreinigende stoffen  Onderzoek identificeert mogelijk doelwit voor streptokokkenvaccin
Onderzoek identificeert mogelijk doelwit voor streptokokkenvaccin Wat is de klonale selectietheorie die van toepassing is op B -cellen?
Wat is de klonale selectietheorie die van toepassing is op B -cellen?  Wat verdwijnen stoffen voordat ze een cel binnenkomen?
Wat verdwijnen stoffen voordat ze een cel binnenkomen?  De eerste waarneming van een materiaal dat een supersolide fase van materie vertoont
De eerste waarneming van een materiaal dat een supersolide fase van materie vertoont  Wat is de straal van een aluminiumatoom 0,143 nm, wat in picometers?
Wat is de straal van een aluminiumatoom 0,143 nm, wat in picometers?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

