
Wetenschap
Wat is de functie van lakmoespapier? Een praktische gids voor zuur-base-testen
Door A.P. Mentzer – Bijgewerkt op 24 maart 2022
Lakmoespapier is een snelle, betrouwbare indicator die laat zien of een oplossing zuur of alkalisch is. Wanneer een stof in water oplost, zorgt de resulterende oplossing ervoor dat het papier van kleur verandert. Hoewel de test snel een ja-of-nee-antwoord geeft, levert deze geen nauwkeurige pH-waarde op.
Zuren en basen
Chemici definiëren zuren en basen op verschillende manieren. Svante Arrhenius, een pionier uit de 19e eeuw, beschreef zuren als verbindingen die waterstofionen (H⁺) in water afgeven, en basen als verbindingen die hydroxide-ionen (OH⁻) vrijgeven. Zoutzuur (HCl) dissocieert bijvoorbeeld en vormt hydronium (H₃O⁺) en chloride (Cl⁻). Ammoniak (NH₃), een base, levert ammonium (NH₄⁺) en hydroxide (OH⁻) op. In alledaagse termen smaken zuren zuur (denk aan citroensap), terwijl basen glad aanvoelen, zoals zeep.
Basisprincipes van de pH-schaal
De pH-schaal kwantificeert de waterstofionenconcentratie met behulp van een negatieve logaritme. Het varieert van 0 tot 14, waarbij 7 neutraal water aangeeft. Waarden onder de 7 geven de zuurgraad aan; boven de 7 geeft de alkaliteit aan. Typische voorbeelden zijn citroensap of maagzuur bij pH ≈2, koffie bij pH ≈5, bloed bij pH ≈7,4, huishoudbleekmiddel bij pH ≈9 en ammoniak bij pH ≈12.
Lakmoespapier
Lakmoespapier is een klassieke zuur-base-indicator. Het komt in rode, blauwe en neutrale (paarse) vormen, elk afgeleid van korstmoskleurstoffen die van kleur veranderen als reactie op de pH. Rood papier wordt blauw in basisoplossingen; blauw papier wordt rood in zure oplossingen. De neutrale strip verandert in rood of blauw, afhankelijk van of de geteste oplossing zuur of alkalisch is.
Een lakmoesproef uitvoeren
Om lakmoespapier te gebruiken, dompelt u een strookje in de vloeistof of brengt u met een pipet een druppeltje aan. Blauw papier wordt rood als het wordt blootgesteld aan een oplossing met een pH van 4–5 of lager. Rood papier wordt blauw als het in contact komt met een base met een pH hoger dan 8. Oplossingen met een pH tussen 5 en 8 zullen een minimale kleurverandering veroorzaken, waardoor het moeilijk wordt ze van elkaar te onderscheiden met alleen lakmoes.
Beperkingen van lakmoespapier
Lakmoespapier blinkt uit in het aangeven van de algemene richting van de zuurgraad of alkaliteit. Het is goedkoop, draagbaar en vereist slechts een klein monstervolume. Het kan echter geen exacte pH-waarde opleveren en is niet effectief voor oplossingen die bijna neutraal zijn (pH 5–8). Voor nauwkeurige metingen wordt een gekalibreerde pH-meter of pH-specifieke indicatoren aanbevolen.
 Hoe wordt regen gevormd?
Hoe wordt regen gevormd?  Locals gewaarschuwd om weg te blijven als Japanse vulkaan uitbarst
Locals gewaarschuwd om weg te blijven als Japanse vulkaan uitbarst Thaise retailers verbieden plastic tassen voor eenmalig gebruik
Thaise retailers verbieden plastic tassen voor eenmalig gebruik Verzuring van de oceaan bereikt niveaus die in 14 miljoen jaar niet zijn gezien
Verzuring van de oceaan bereikt niveaus die in 14 miljoen jaar niet zijn gezien Wat gebeurt er met de waarde van onroerend goed als steden de infrastructuur versterken ter bescherming tegen klimaatverandering?
Wat gebeurt er met de waarde van onroerend goed als steden de infrastructuur versterken ter bescherming tegen klimaatverandering?
Hoofdlijnen
- Hoe verschillen meiose en mitose zowel?
- Wat is mRNA? u moet op de hoogte zijn van het belangrijkste ingrediënt in sommige COVID-19-vaccins
- Is mitochondria een functie of structuur?
- Wat zijn de lagen op buiten een celmembraan genoemd?
- Groeit gist in LB Agar?
- Wat zijn twee soorten RNA?
- Welke vorm zijn dierencellen?
- Waar is weefsel van gemaakt?
- Prokaryoten worden geclassificeerd als behorend tot twee verschillende domeinen Wat de domeinen?
- Onderzoekers onthullen moleculaire basis van visie

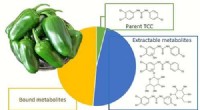
- Peperplant zuigt antibioticum voor persoonlijke verzorging op
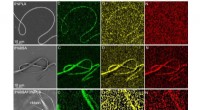
- Biofysici mengen onverenigbare componenten tot één nanovezel
- De verrassende wetenschap achter waarom sinaasappelschilsap ballonnen laat knappen

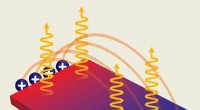
- Exciplex-emissie waargenomen over veel langere afstanden dan eerder voor mogelijk werd gehouden
 Wat is mechanische en chamische verwering?
Wat is mechanische en chamische verwering?  Wat zijn zowel hoge massa als lage volwassen sterren geclassificeerd als?
Wat zijn zowel hoge massa als lage volwassen sterren geclassificeerd als?  Welke chemische stof leeft?
Welke chemische stof leeft?  Wetenschapsprojecten: ijs tegen smelten beschermen
Wetenschapsprojecten: ijs tegen smelten beschermen Wat is de structurele koolhydraten in planten?
Wat is de structurele koolhydraten in planten?  Hoe wijzigen gletsjers een vallei aan?
Hoe wijzigen gletsjers een vallei aan?  Welke stof wordt gebruikt voor snelle energie?
Welke stof wordt gebruikt voor snelle energie?  Een demografisch percentage berekenen
Een demografisch percentage berekenen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

