
Wetenschap
Hoe temperatuur de pH van zuiver water beïnvloedt
Door Claire Gillespie | Bijgewerkt op 24 maart 2022
smileitsmccheeze/iStock/GettyImages
De pH-schaal kwantificeert hoe zuur of alkalisch een oplossing is. Zuiver, gedestilleerd water is neutraal en heeft een pH van 7. Wanneer water wordt verwarmd, daalt de pH een heel klein beetje; een effect dat zo subtiel is dat standaard pH-strips dit meestal over het hoofd zien.
TL;DR
In zuiver water stijgt de temperatuur bij lagere pH en bij lagere temperaturen stijgt deze, maar de verschuivingen zijn te klein voor de meeste routinematige pH-testen.
De pH-schaal begrijpen
De pH-waarde weerspiegelt de concentratie waterstofionen (H⁺) in een oplossing. Elke stap op de schaal met een geheel getal vertegenwoordigt een tienvoudige verandering in de H⁺-concentratie. Een verschuiving van pH 5 naar 6 duidt dus op een tienvoudige vermindering van waterstofionen.
Temperatuur en chemisch evenwicht
Het principe van Le Châtelier stelt dat een systeem in evenwicht zal verschuiven om een verstoring tegen te gaan. Het verhogen van de temperatuur van water duwt het zelf-ionisatie-evenwicht naar de eindproducten - meer H⁺ en OH⁻. Bijgevolg daalt de totale pH. Het verhogen van de temperatuur van 0 °C naar 10 °C verlaagt bijvoorbeeld de pH van zuiver water met ongeveer 0,2 eenheden. Het verlagen van de temperatuur heeft het omgekeerde effect.
Waarom de pH niet gelijk is aan de zuurgraad in zuiver water
Een lagere pH betekent niet dat het water zuurder wordt; de concentraties waterstof- en hydroxide-ionen blijven gelijk, waardoor de oplossing neutraal blijft. Bij 25 °C heeft zuiver water een pH van 7. Bij verhitting tot 100 °C daalt de pH naar 6,14. Nog steeds neutraal op de schaal, maar iets lager.
 Hoe het oudste bewijs van beweging kan veranderen wat we weten over het leven op aarde
Hoe het oudste bewijs van beweging kan veranderen wat we weten over het leven op aarde Klimaatverandering zal de ecosystemen van Queensland onherkenbaar maken - het is aan ons of we dat willen stoppen
Klimaatverandering zal de ecosystemen van Queensland onherkenbaar maken - het is aan ons of we dat willen stoppen Recordhoeveelheid hernieuwbare energiecapaciteit toegevoegd in 2016:UN
Recordhoeveelheid hernieuwbare energiecapaciteit toegevoegd in 2016:UN Een ton fossiele koolstof is niet hetzelfde als nieuwe bomen:waarom compensaties ons niet kunnen redden
Een ton fossiele koolstof is niet hetzelfde als nieuwe bomen:waarom compensaties ons niet kunnen redden  Wat maakt deel uit van een plant waar water reist?
Wat maakt deel uit van een plant waar water reist?
Hoofdlijnen
- Wat is een enkel gestrand nucleïnezuur dat een rol speelt in eiwitsynthese.
- Wat is de wetenschapsdefinitie voor Repel?
- Wat wordt bedoeld met biologische fitheid?
- Wat wordt er in alleen plantencellen gevonden die fotosynthese ondergaan?
- Waarom ondersteunen de lichaamsstructuren van sommige soorten de theorieën?
- Hoeveel verschillende combinaties van maternale en vaderlijke chromosomen kunnen worden verpakt in gameten gemaakt door een organisme met een diploïde nummer 8?
- Welke organellen buiten de celkern bevatten genetisch materiaal?
- Wat is het doel van reproductie?
- Hoe groene algen celdelingen tellen, belicht een belangrijke stap die nodig is voor de evolutie van meercellig leven
- Milieuvriendelijk textiel is gemakkelijk en goedkoop te vervaardigen

- Toekomstige auto's kunnen gemaakt worden van revolutionair nieuw materiaal

- Batterijprestaties beoordelen:in vergelijking met wat?

- Licht biedt controle voor 3D-printen met meerdere materialen

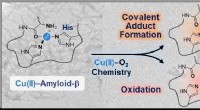
- Coördinatiechemie en de ziekte van Alzheimer
 Is getijdenenergie een directe of indirecte vorm van zonne -energie?
Is getijdenenergie een directe of indirecte vorm van zonne -energie?  Ontdekker van het skelet van Lucy hoopt te ontdekken wat ons menselijk heeft gemaakt
Ontdekker van het skelet van Lucy hoopt te ontdekken wat ons menselijk heeft gemaakt  De laserdoorbraak die technologie nog sneller zou kunnen maken
De laserdoorbraak die technologie nog sneller zou kunnen maken Wordt het alluviale conglomeraat Rock Record Magnetic Field op tijd gevormd?
Wordt het alluviale conglomeraat Rock Record Magnetic Field op tijd gevormd?  Ionische bindingen:sterkte, vorming en eigenschappen - een uitgebreide uitleg
Ionische bindingen:sterkte, vorming en eigenschappen - een uitgebreide uitleg  Nieuw model voorspelt locaties van biologische hotspots in de oceaan
Nieuw model voorspelt locaties van biologische hotspots in de oceaan Airbnb-hosts in universiteitssteden verhogen de prijzen van gamedagen om rivaliserende fans af te schrikken
Airbnb-hosts in universiteitssteden verhogen de prijzen van gamedagen om rivaliserende fans af te schrikken Hoe wordt ook negatieve versnelling genoemd?
Hoe wordt ook negatieve versnelling genoemd?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

