
Wetenschap
Ionische bindingen:sterkte, vorming en eigenschappen - een uitgebreide uitleg
* Elektrostatische aantrekkingskracht: Ionische bindingen worden gevormd door de elektrostatische aantrekking tussen tegengesteld geladen ionen. Deze aantrekkingskracht is erg sterk, vooral als de ionen hoge ladingen hebben.
* Roosterstructuur: Ionische verbindingen vormen een kristalroosterstructuur, waarbij ionen in een regelmatig, herhalend patroon zijn gerangschikt. Deze structuur maximaliseert de elektrostatische aantrekkingskracht tussen ionen, waardoor de binding nog sterker wordt.
* Hoge smelt- en kookpunten: De sterke elektrostatische krachten in ionische bindingen vereisen veel energie om te overwinnen. Dit is de reden waarom ionische verbindingen doorgaans hoge smelt- en kookpunten hebben.
* Oplosbaarheid in polaire oplosmiddelen: Ionische verbindingen hebben de neiging op te lossen in polaire oplosmiddelen (zoals water) omdat de polaire oplosmiddelmoleculen de ionen kunnen omringen en scheiden, waardoor de ionische bindingen worden verbroken.
Waarom ze in sommige contexten "zwak" lijken:
* Oplosbaarheid: Hoewel ionische bindingen sterk zijn, kunnen ze worden verbroken door polaire oplosmiddelen. Dit is de reden waarom ionische verbindingen in water kunnen oplossen, waardoor ze in deze context ‘zwak’ lijken.
* Hydratatie: Wanneer ionische verbindingen in water oplossen, worden de ionen omgeven door watermoleculen (hydratatie). Dit kan de elektrostatische aantrekkingskracht tussen de ionen enigszins verzwakken.
Samengevat: Ionische bindingen zijn inherent sterk vanwege de krachtige elektrostatische aantrekkingskracht tussen ionen. Ze kunnen echter worden beïnvloed door factoren als oplosbaarheid en hydratatie, waardoor ze in bepaalde situaties ‘zwak’ kunnen lijken.
 Hoe kunt u de producten van fotosynthese gebruiken om niveaus schadelijke luchtverontreinigende stoffen te verminderen?
Hoe kunt u de producten van fotosynthese gebruiken om niveaus schadelijke luchtverontreinigende stoffen te verminderen?  Nieuwe aanpak kan autoriteiten helpen sneller te reageren op radiologische dreigingen in de lucht
Nieuwe aanpak kan autoriteiten helpen sneller te reageren op radiologische dreigingen in de lucht Wat maakt regen zuur?
Wat maakt regen zuur?  Onderzoekers maken theoretische voorspelling van 2-D halfgeleider tindioxide
Onderzoekers maken theoretische voorspelling van 2-D halfgeleider tindioxide De rol van glycerol in levende cellen:belang en functies
De rol van glycerol in levende cellen:belang en functies
 Java's beschermende mangroven gesmoord door plastic afval
Java's beschermende mangroven gesmoord door plastic afval Wetenschappers afluisteren vulkanisch gerommel af om uitbarstingen te voorspellen
Wetenschappers afluisteren vulkanisch gerommel af om uitbarstingen te voorspellen In welke categorie wetenschap vallen vervuiling en recycling onder?
In welke categorie wetenschap vallen vervuiling en recycling onder?  Atmosferische aërosolvorming uit biogene dampen wordt sterk beïnvloed door luchtverontreinigende stoffen
Atmosferische aërosolvorming uit biogene dampen wordt sterk beïnvloed door luchtverontreinigende stoffen Herbeoordeling klimaatverandering roept op tot een nuchterder discours
Herbeoordeling klimaatverandering roept op tot een nuchterder discours
Hoofdlijnen
- Wat is een voorbeeld van katabolisme?
- Welke biomen ondersteunen het grootste aantal soorten?
- Is de symbiotische relatie waarin het ene organisme profiteert, maar het andere wordt geschaad?
- Hoe komt cytokenesis voor in de meeste dierlijke cellen?
- Herstel van iconische inheemse vogel veroorzaakt problemen in stedelijke gebieden
- Stages of Mitosis (Cell Division)
- Waarom worden cellen beschouwd als de basiseenheden van het leven?
- Welk deel van de ademhaling produceert de meeste ATP?
- Worden we echt wijzer met de jaren?
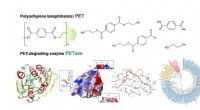
- Structureel inzicht in het moleculaire mechanisme van PET-degradatie
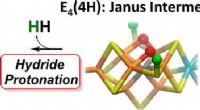
- De weg vrijmaken voor zuinige meststoffen
- Zijn antivitamines de nieuwe antibiotica?

- Genetische oorzaak van ALS en frontotemporale dementie geblokkeerd door RNA-bindende verbinding

- Nieuw scheidingsproces voor belangrijk radiodiagnostisch middel vermindert radioactief afval

 Wetenschappers construeren organo-fosfatische schelpen van brachiopoden
Wetenschappers construeren organo-fosfatische schelpen van brachiopoden  Wat zijn de intermoleculaire krachten van HClO?
Wat zijn de intermoleculaire krachten van HClO?  Aeolus werpt licht op polaire vortex
Aeolus werpt licht op polaire vortex Wat was ontdekking op elektriciteit?
Wat was ontdekking op elektriciteit?  Wat voor soort kracht wordt getoond als er lucht uit de nek snelt, een ballon veroorzaakt om te bewegen?
Wat voor soort kracht wordt getoond als er lucht uit de nek snelt, een ballon veroorzaakt om te bewegen?  Hoeveel mol O in CUSO4?
Hoeveel mol O in CUSO4?  Waarom worden mensen astronomen?
Waarom worden mensen astronomen?  Machine learning versnelt de ontdekking van hoogwaardige metaaloxidekatalysatoren
Machine learning versnelt de ontdekking van hoogwaardige metaaloxidekatalysatoren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

