
Wetenschap
Natrium's Single Valence Electron:wat het betekent voor chemische reactiviteit
cookelma/iStock/GettyImages
Natrium (Na) is een alkalimetaal met 11 elektronen. Slechts één van deze elektronen bevindt zich in de buitenste, derde schil, waardoor dit het enige valentie-elektron is. Omdat de valentieschil de eerste is die interactie aangaat tijdens een chemische reactie, dicteert dit eenzame elektron grotendeels de reactiviteit van natrium en de soorten verbindingen die het vormt.
TL;DR
Natrium heeft één valentie-elektron. De binnenste schillen zijn gevuld (2+8 elektronen), terwijl de buitenste schil er slechts één bevat. Dit zorgt voor de hoge reactiviteit en de neiging om ionische bindingen te vormen.
Valentie-elektronen en chemische reactiviteit
Elektronenschillen volgen een eenvoudige regel:de eerste kan 2 elektronen bevatten, de tweede 8 en de derde 18 (twee, zes en tien subschillen). Een stabiel atoom zoekt naar een volledig gevulde buitenschil. Een element is het meest reactief als de buitenste schil één elektron heeft of één elektron tekortschiet – omstandigheden die de elektronenoverdracht eenvoudig en energetisch gunstig maken.
De reactiviteit van natrium met andere elementen
Met nog maar één elektron over, doneert natrium dat elektron gemakkelijk aan elementen die er nog één nodig hebben om een volledige buitenschil te bereiken. Wanneer natrium bijvoorbeeld chloor (Cl) tegenkomt, waarvoor één extra elektron nodig is, ontstaan bij de overdracht Na⁺- en Cl⁻-ionen. De elektrostatische aantrekking tussen de tegengesteld geladen ionen produceert de stabiele ionische verbinding natriumchloride (tafelzout).
In het periodiek systeem bezitten alkalimetalen (groep 1) één valentie-elektron, terwijl halogenen (groep 17) er één nodig hebben om hun buitenste schil te voltooien, waardoor ze de belangrijkste partners zijn voor natrium.
Valentie-elektronen in natriumionen in oplossing
Wanneer natriumchloride in water oplost, dissocieert het in Na⁺- en Cl⁻-ionen. Het natriumion behoudt een volledig bezette buitenste schil van acht elektronen en heeft een lading van +1. Het chloride-ion, dat het valentie-elektron van natrium heeft geaccepteerd, bezit ook een volledige buitenschil en heeft een lading van -1. Als de schillen van beide ionen tevreden zijn, blijven ze inert in de oplossing.
 Welke stof wordt opgebruikt tijdens fotosynthese?
Welke stof wordt opgebruikt tijdens fotosynthese?  Als 40 gram natriumhydroxide en 3 waterstofgas worden geproduceerd wanneer 27 metaal wordt verbruikt, hoeveel vloeibaar water moet zijn toegevoegd?
Als 40 gram natriumhydroxide en 3 waterstofgas worden geproduceerd wanneer 27 metaal wordt verbruikt, hoeveel vloeibaar water moet zijn toegevoegd?  Inzicht in het soortelijk gewicht en het anilinepunt in olie
Inzicht in het soortelijk gewicht en het anilinepunt in olie  Isotopen zoeken
Isotopen zoeken  Welke richting is fluorietsplitsing?
Welke richting is fluorietsplitsing?
 De beschikbaarheid van water is veranderd, en de mens is de schuldige
De beschikbaarheid van water is veranderd, en de mens is de schuldige Frequente extreme bosbranden zijn onze nieuwe realiteit:we moeten leren leven met met rook gevulde lucht
Frequente extreme bosbranden zijn onze nieuwe realiteit:we moeten leren leven met met rook gevulde lucht Hoe loopt een hond? Verrassend genoeg weten velen van ons het niet echt
Hoe loopt een hond? Verrassend genoeg weten velen van ons het niet echt  Vervuiling van afvalwater:waarom de Britse waterindustrie kapot is
Vervuiling van afvalwater:waarom de Britse waterindustrie kapot is Dit enzym stelde het leven in staat een vijandige aarde te veroveren
Dit enzym stelde het leven in staat een vijandige aarde te veroveren
Hoofdlijnen
- Welke bacteriën leven in moerassen?
- Hoe lijkt een model op het echte object dat het vertegenwoordigt?
- Indringende vraag:Waarom worden albino's altijd als schurken neergezet?
- Waarom kan een cel veel rRNA maken, maar slechts één kopie van het DNA?
- De cel wegen:voor het eerst meten hoe afzonderlijke cellen massa accumuleren (met video)
- Wat vertegenwoordigt het nucleaire membraan?
- Wat is nephoning en waarom hebben de officiële tests dit niet opgepikt?
- Studie beantwoordt een al lang bestaand mysterie over slangenpredatie
- Wat is de wetenschappelijke naam voor een organisme komt vandaan
- Uitvinding van vormveranderend textiel dat alleen wordt aangedreven door lichaamswarmte
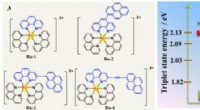
- Fijnafstemming van de aangeslagen toestand van Ru(II)-fotosensibilisatoren voor het stimuleren van de omzetting van kooldioxide
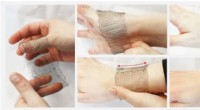
- Het giswerk uit de forensische analyse van vingerafdrukken halen

- Wat als we krachtige medicijnen zouden kunnen ontwerpen zonder ongewenste bijwerkingen?

- Hoe een reactie in een chemische vergelijking te identificeren

 Wat is het spul dat groeit op rotsen in grotten geroepen?
Wat is het spul dat groeit op rotsen in grotten geroepen?  Chemici maken zelfassemblerend materiaal met een reeks nieuwe eigenschappen
Chemici maken zelfassemblerend materiaal met een reeks nieuwe eigenschappen Waar of niet waar. Onze zon is een witte dwergster?
Waar of niet waar. Onze zon is een witte dwergster?  Onthulling van de rotte landbouwbedrijven in Brazilië
Onthulling van de rotte landbouwbedrijven in Brazilië Waar bestaat het cytoplasma uit?
Waar bestaat het cytoplasma uit?  6 Wanneer een appel van een boom naar de grond valt, beginnend met kinetische energie en het eindigen van zwaartekrachtpotentieel zijn beide gelijk aan?
6 Wanneer een appel van een boom naar de grond valt, beginnend met kinetische energie en het eindigen van zwaartekrachtpotentieel zijn beide gelijk aan?  Wat is de minerale samenstelling van moddersteen?
Wat is de minerale samenstelling van moddersteen?  Hoe verwerft men rotsmonsters van de oceaanbodem?
Hoe verwerft men rotsmonsters van de oceaanbodem?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

