
Wetenschap
Het half-equivalentiepunt op een titratiecurve lokaliseren:een praktische gids
Door Chris Deziel | Bijgewerkt op 24 maart 2022
Tijdens een typische zuur-base-titratie wordt de zich ontwikkelende pH uitgezet tegen het toegevoegde volume titrant. De resulterende curve begint met een geleidelijke stijging en wordt vervolgens scherp steiler op het equivalentiepunt waar al het zuur is geneutraliseerd. Het punt precies halverwege tussen de oorsprong en het equivalentiepunt op de x-as is het halve equivalentiepunt. Op dit moment is de pH van de oplossing gelijk aan de dissociatieconstante van het zuur, pKa.
Het half-equivalentiepunt lokaliseren
De titratie wordt gecontroleerd met behulp van een kleurveranderende indicator, een pH-meter, een potentiometer of spectroscopische technieken. Terwijl de base wordt toegevoegd, stijgt de pH langzaam totdat deze het equivalentiepunt bereikt; daarna stijgt de curve steil. Na het equivalentievolume loopt de helling weer taps toe en neemt de pH geleidelijker toe.
Identificeer het equivalentiepunt door het buigpunt te lokaliseren waar de curve overgaat van de zachte naar de steile helling. Zodra dat volume bekend is, is het halve-equivalentiepunt eenvoudigweg het middelpunt op de x-as tussen het nulvolume en het equivalentievolume.
Betekenis van het half-equivalentiepunt
De Henderson-Hasselbalch-vergelijking, pH =pKa + log([A⁻]/[HA]), koppelt de zuur-base-verhouding aan de pH. Op het half-equivalentiepunt zijn de concentraties van het zuur (HA) en de geconjugeerde base (A⁻) gelijk, waardoor de verhouding één is. Bijgevolg is log1 =0 en wordt de vergelijking gereduceerd tot pH =pKa. Door een verticale lijn naar het half-equivalentievolume en een horizontale lijn naar de y-as te trekken, kan de pKa daarom direct uit de curve worden afgelezen.
Het kennen van het halve-equivalentiepunt is cruciaal voor het karakteriseren van zwakke zuren, het ontwerpen van buffersystemen en het valideren van titratieprotocollen.
 Wat is de oude Hebreeuwse eenheid van vloeibaar volume gelijk aan tien baden?
Wat is de oude Hebreeuwse eenheid van vloeibaar volume gelijk aan tien baden?  De moleculaire structuur van een bosaroma gedeconstrueerd
De moleculaire structuur van een bosaroma gedeconstrueerd Het ontrafelen van de structurele dynamiek van fotosysteem II met femtoseconde röntgenkristallografie
Het ontrafelen van de structurele dynamiek van fotosysteem II met femtoseconde röntgenkristallografie  Wat is het hoofdbestanddeel van Teflon?
Wat is het hoofdbestanddeel van Teflon?  Samengestelde woorden versus samengestelde woorden uit één woord:een duidelijke uitleg
Samengestelde woorden versus samengestelde woorden uit één woord:een duidelijke uitleg
 Hoe is de aardwetenschap gerelateerd aan de fysieke wetenschap?
Hoe is de aardwetenschap gerelateerd aan de fysieke wetenschap?  Maakt erosie het moeilijk voor planten?
Maakt erosie het moeilijk voor planten?  Nieuw raamwerk om onzekerheid in waterbeheer aan te pakken
Nieuw raamwerk om onzekerheid in waterbeheer aan te pakken Kinderen krijgen tijdens de schoolloop drie keer meer luchtvervuiling te verwerken
Kinderen krijgen tijdens de schoolloop drie keer meer luchtvervuiling te verwerken Wat de SCOTUS-uitspraak over EPA en emissies betekent voor klimaatverandering
Wat de SCOTUS-uitspraak over EPA en emissies betekent voor klimaatverandering
Hoofdlijnen
- Wanneer dupliceren chromosomen tijdens een cellevenscyclus?
- Wat betekent de term biotechnologie?
- Een online ontmoeting met je hond? Studie test het vermogen van honden om acties te imiteren die worden waargenomen op videoprojecties
- Welk niveau van biologische organisatie omvat de grootste totale aantal soorten?
- Onderzoekers werpen licht op hoe een belangrijk ingrediënt voor leven zich in de ruimte kan vormen
- RNA-productie:transcriptie en RNA-polymerase begrijpen
- Welk gebied produceert cellen in een plant?
- Wat doet ethanol in een DNA-extractie?
- Wie is de vader van de moderne biotechnologie?
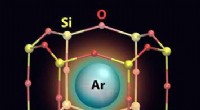
- Bestuderen van argongas gevangen in een tweedimensionale reeks kleine kooien
- Nieuwe techniek geeft polyurethaanafval een tweede leven

- Nieuwe stabiele vorm van plutonium ontdekt

- Waardoor smaakt en ruikt de Appalachian truffel heerlijk?

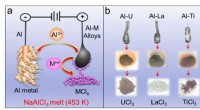
- Wetenschappers stellen IAP-proces voor voor scheiding van aluminiumlegeringen
 Planeetverwarring kan de verkenning van aardachtige exoplaneten vertragen
Planeetverwarring kan de verkenning van aardachtige exoplaneten vertragen Wat is 50 graden F in Celsius?
Wat is 50 graden F in Celsius?  Een 16 Newton Net Force wordt toegepast op een 2-kg massa Wat de versnelling van de massa?
Een 16 Newton Net Force wordt toegepast op een 2-kg massa Wat de versnelling van de massa?  Wereldwijde onvrede over democratie op recordhoogte, nieuw rapport onthult
Wereldwijde onvrede over democratie op recordhoogte, nieuw rapport onthult Hoeveel valentie-elektronen zitten er in een Fr-atoom?
Hoeveel valentie-elektronen zitten er in een Fr-atoom?  Met zeep betrapt:begrijpen hoe zeepmoleculen eiwitten helpen om in en uit vorm te komen
Met zeep betrapt:begrijpen hoe zeepmoleculen eiwitten helpen om in en uit vorm te komen Waar wordt de minerale diamant gevonden?
Waar wordt de minerale diamant gevonden?  Noem een bacterie die geen ziekte veroorzaakt?
Noem een bacterie die geen ziekte veroorzaakt?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

