
Wetenschap
Ionen versus elektrolyten:hun rol in de biologie en de industrie begrijpen
Door Michael Judge
Bijgewerkt op 24 maart 2022
Ionen
In de scheikunde is een ion een geladen soort die wordt gevormd wanneer een atoom of een groep atomen elektronen verliest of wint. Terwijl een neutraal atoom gelijke aantallen protonen (positief geladen) en elektronen (negatief geladen) bevat, zorgt de verwijdering of toevoeging van een of meer elektronen voor een netto lading. Deze fundamentele eigenschap ligt ten grondslag aan talloze biologische processen – zoals de overdracht van zenuwimpulsen – en industriële toepassingen zoals galvaniseren.
Elektrolyten
Een elektrolyt is elke verbinding die ionen afgeeft wanneer deze in water wordt opgelost. Tijdens het oplossen breken de chemische bindingen in de opgeloste stof, waardoor vrij bewegende geladen deeltjes ontstaan die worden gestabiliseerd door de enigszins polaire aard van watermoleculen. Dit fenomeen zorgt ervoor dat elektrolyten elektriciteit kunnen geleiden, een principe dat in alles wordt uitgebuit, van het menselijke zenuwstelsel tot moderne batterijen.
Soorten elektrolyten
Elektrolyten worden gecategoriseerd op basis van de mate van dissociatie in oplossing:
- Sterke elektrolyten volledig dissociëren, waardoor er vrijwel geen ongedissocieerde moleculen overblijven. Veel voorkomende voorbeelden zijn onder meer natriumchloride (NaCl), dat Na⁺- en Cl⁻-ionen produceert, en zoutzuur (HCl), dat H⁺ en Cl⁻ oplevert.
- Zwakke elektrolyten gedeeltelijk dissociëren, zodat een aanzienlijk deel intact blijft. Azijnzuur (CH₃COOH) is een typische zwakke elektrolyt, die een beperkte hoeveelheid acetaat- (CH₃COO⁻) en H⁺-ionen produceert.
Elektrolyttoepassingen
De door elektrolyten gegenereerde ionen zijn essentieel voor tal van functies:
- Fysiologische processen – Het menselijk lichaam is afhankelijk van elektrolyten zoals NaCl om de cellulaire homeostase, zenuwgeleiding en vochtbalans te behouden.
- Energieopslag – Batterijen gebruiken elektrolytoplossingen die ionen bevatten, zoals Zn²⁺ en Cu²⁺ om de ladingsoverdracht tussen elektroden te vergemakkelijken.
- Industriële chemie – Elektrolyten, zowel zuur als basisch, zijn een integraal onderdeel van de metaalverwerking, chemische synthese en de vervaardiging van alledaagse producten.
 Welke vaste stof reageert met verdund zoutzuur onder vorming van koolstofdioxide?
Welke vaste stof reageert met verdund zoutzuur onder vorming van koolstofdioxide?  Hoeveel valentie -elektronen zijn er in fosforzuur?
Hoeveel valentie -elektronen zijn er in fosforzuur?  Microcapsules krijgen een nieuwe kracht - het wegvangen van reactieve zuurstofsoorten
Microcapsules krijgen een nieuwe kracht - het wegvangen van reactieve zuurstofsoorten Wat is de conversie van temperatuurmassa volume en dichtheid?
Wat is de conversie van temperatuurmassa volume en dichtheid?  Nadat atomen en moleculen van gassen worden verwarmd, gaan ze weg van de hitte. Wat neemt hun plaats aan?
Nadat atomen en moleculen van gassen worden verwarmd, gaan ze weg van de hitte. Wat neemt hun plaats aan?
 Nieuwe zuiveringstechnieken voor gezondere aquatische ecosystemen
Nieuwe zuiveringstechnieken voor gezondere aquatische ecosystemen Vraag en antwoord:Uit onderzoek blijkt het belang van actieplannen om natuurreservaten te beschermen om te ontsnappen aan de zomerse hitte
Vraag en antwoord:Uit onderzoek blijkt het belang van actieplannen om natuurreservaten te beschermen om te ontsnappen aan de zomerse hitte  Leven en dood van Irma:einde van 2 weken van woede en verwoesting
Leven en dood van Irma:einde van 2 weken van woede en verwoesting De tsunami in Alaska die golven veroorzaakte die zo hoog waren als de Space Needle van Seattle
De tsunami in Alaska die golven veroorzaakte die zo hoog waren als de Space Needle van Seattle Azië moet stoppen met kolenverslaving:VN-chef
Azië moet stoppen met kolenverslaving:VN-chef
Hoofdlijnen
- Waar zijn hormonen een voorbeeld van?
- Wat is de studie van lichaamsweefsel genaamd beginnend met bio?
- Wat zijn de 4 belangrijkste groepen algen?
- De plantencelkern:het controlecentrum van de cel begrijpen
- Waarom is een blad een orgel?
- Wat draagt de genetische informatie van Nulceus naar cytoplasma?
- Wat is de functie van circulair DNA in bacteriën?
- Celdeling die vervolgens volgt, biedt nieuwe cellen zodat wat kan gebeuren?
- Wat is de juiste definitie als het metabolisme?
- Schadelijke moleculen detecteren met licht

- Een zoutoplossing voor het ontzilten van pekel

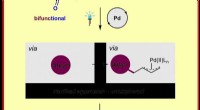
- Oude overgangsmetalen nieuwe trucjes leren:scheikundigen activeren palladiumkatalyse door licht
- Vingerafdrukken missen wetenschappelijke basis voor rechtszekerheid

- Nieuw inzicht in hoe stamcellen interageren met borstkankercellen
 Chemische reacties:reactanten en producten begrijpen
Chemische reacties:reactanten en producten begrijpen  Wat is de snelheid van een object dat na 5 seconden van een klif is afgezet en geen luchtweerstand met initiële 0 ms?
Wat is de snelheid van een object dat na 5 seconden van een klif is afgezet en geen luchtweerstand met initiële 0 ms?  Welke ingrediënten gebruikt fotosynthese?
Welke ingrediënten gebruikt fotosynthese?  Hoe wordt de energie van een aardbeving opgeslagen vóór de aardbeving?
Hoe wordt de energie van een aardbeving opgeslagen vóór de aardbeving?  Nieuwe retailtools zijn bedoeld om het winstdilemma van e-commerce op te lossen
Nieuwe retailtools zijn bedoeld om het winstdilemma van e-commerce op te lossen Wetenschapsleiders roepen op tot empirisch onderbouwd beleid
Wetenschapsleiders roepen op tot empirisch onderbouwd beleid De Noordelijke IJszee kan in 2044 een deel van het jaar ijsvrij zijn
De Noordelijke IJszee kan in 2044 een deel van het jaar ijsvrij zijn Amerikaans-Brits trio wint Nobelprijs voor geneeskunde voor ontdekking van hepatitis C
Amerikaans-Brits trio wint Nobelprijs voor geneeskunde voor ontdekking van hepatitis C
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

