
Wetenschap
Een praktische gids voor de zes kerntypen van chemische reacties
Door Lan Luo
Bijgewerkt op 30 augustus 2022
Jardul/iStock/GettyImages
Chemische reacties zijn een integraal onderdeel van de moderne technologie en het dagelijks leven, van het aandrijven van motoren tot het brouwen van dranken. Ze sturen ook natuurlijke processen aan, zoals fotosynthese en verwering van gesteenten.
Drie brede categorieën reacties
Fysieke reacties alleen een verandering in de toestand of de fysieke structuur met zich meebrengen, zonder wijziging van de chemische identiteit van de stoffen. Bevriezend water bijvoorbeeld:
H₂O(l) → H₂O(s)
Chemische reacties transformeren reactanten in nieuwe producten door de herschikking van atomen. Een klassiek voorbeeld is het oplossen van CO₂ in water om koolzuur te vormen:
CO₂(g) + H₂O(l) → H₂CO₃(aq)
Kernreacties veranderingen in atoomkernen met zich meebrengen, zoals Rutherfords transmutatie van stikstof:
¹⁴N + α → ¹⁷O + p
De zes belangrijkste chemische reactietypen
Synthese (combinatie)reactie
Twee of meer reactanten vormen samen één enkel, complexer product. Algemene vorm:
A + B → AB
Voorbeelden:
Fe(s) + S(s) → FeS(s)
2Na(s) + Cl₂(g) → 2NaCl(s)
Ontbindingsreactie
Een enkele complexe reactant valt uiteen in twee of meer eenvoudiger producten. Algemene vorm:
AB → A + B
Voorbeelden:
H₂O(l) → H₂(g) + O₂(g) (elektrolyse)
H₂CO₃(aq) → H₂O(l) + CO₂(g) (thermische ontleding)
Enkele verplaatsingsreactie (vervanging)
Een element verdringt een ander element uit een verbinding. Algemene vorm:
A + BC → AC + B
Voorbeelden:
Mg(s) + 2HCl(aq) → H₂(g) + MgCl₂(aq)
Mg(s) + 2H₂O(l) → H₂(g) + Mg(OH)₂(aq)
Dubbele verplaatsingsreactie (metathese)
Kationen en anionen wisselen van partner en vormen twee nieuwe verbindingen. Algemene vorm:
AB + CD → AD + CB
Voorbeelden:
BaCl₂ + MgSO₄ → BaSO₄ + MgCl₂
Pb(NO₃)₂ + 2KI → PbI₂ + 2KNO₃
Verbrandingsreactie
Een exotherm redoxproces waarbij een brandstof reageert met zuurstof, waarbij voornamelijk CO₂ en H₂O ontstaat. Volledige verbranding:
4CxHy + (4x+y)O₂ → 4xCO₂ + 2yH₂O + warmte
Specifieke voorbeelden:
CH₄ + 2O₂ → CO₂ + 2H₂O + warmte (≈891kJmol⁻¹)
C₁₀H₈ + 12O₂ → 10CO₂ + 4H₂O + warmte
CH₃OH + O₂ → CO₂ + 2H₂O + warmte
Onvolledige verbranding vindt plaats wanneer de O₂ beperkt is, waardoor CO, roet of andere bijproducten ontstaan.
Zuur-base-reactie
Een neutralisatieproces waarbij een zuur reageert met een base om een zout en water te vormen. Het is een speciaal geval van dubbele verplaatsing:
HA + BOH → BA + H₂O
Voorbeelden:
Ca(OH)₂ + 2HCl → CaCl₂ + 2H₂O
CH₃COOH + NaHCO₃ → CH₃COONa + H₂O + CO₂
Waarom het begrijpen van deze typen belangrijk is
Het herkennen van het reactiepatroon helpt scheikundigen en ingenieurs bij het voorspellen van producten, het optimaliseren van omstandigheden en het garanderen van de veiligheid, vooral bij industriële verbranding of farmaceutische synthese.
 Echte truffels opsnuiven
Echte truffels opsnuiven Hoe verschillen vaste stoffen, vloeistoffen en gassen, deeltjes?
Hoe verschillen vaste stoffen, vloeistoffen en gassen, deeltjes?  Zorgt het pH -niveau in zuur ervoor dat het door dingen smelt?
Zorgt het pH -niveau in zuur ervoor dat het door dingen smelt?  Is Uranium een voorbeeld van een fossiele brandstof?
Is Uranium een voorbeeld van een fossiele brandstof?  Beschrijf twee manieren waarop radioactieve isotopen worden gebruikt in biomedisch onderzoek?
Beschrijf twee manieren waarop radioactieve isotopen worden gebruikt in biomedisch onderzoek?
 Vissende nomaden:karpers bijeendrijven op het Thousand Island-meer in China
Vissende nomaden:karpers bijeendrijven op het Thousand Island-meer in China Interessante feiten over de Hackberry Tree
Interessante feiten over de Hackberry Tree  Welke zintuigen zijn nuttiger bij het beschrijven van kwalitatieve eigenschappen?
Welke zintuigen zijn nuttiger bij het beschrijven van kwalitatieve eigenschappen?  Mangroven essentieel voor milieusanering
Mangroven essentieel voor milieusanering Van permafrostmicroben tot overlevende zangvogels, onderzoeksprojecten zijn ook slachtoffer van pandemie
Van permafrostmicroben tot overlevende zangvogels, onderzoeksprojecten zijn ook slachtoffer van pandemie
Hoofdlijnen
- Wie is er bekend om ontdekkingen in radioactiviteit?
- Welke organel houdt samen kern?
- Welke structuur is verantwoordelijk voor de uitscheiding van het meeste cellulaire afvalstructuur?
- Welke verpakkingen pakketten eiwitten en transporteert eiwitten in een cel?
- Wat is de betekenis van biodeversity?
- Is evolutie intelligenter dan we dachten?
- De allereerste tagging van Amazone-dolfijnen om de inspanningen voor natuurbehoud te stimuleren
- Wat is een zelfstandig naamwoord voor een beluchting?
- In welke cel is de nauwkeurige overdracht van informatie het belangrijkst?
- Pig-Pen-effect:het mengen van huidolie en ozon kan een persoonlijke vervuilingswolk veroorzaken
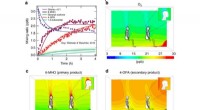
- Druppels beklimmen kan leiden tot efficiëntere waterwinning

- Nieuwe chemische hulpmiddelen om biomoleculen te wijzigen en te bestuderen
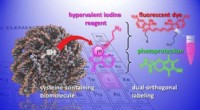
- Chemici komen een stap dichter bij het nabootsen van de natuur met assemblage van nieuwe 3D-structuren

- Ontwikkelen van een breed temperatuurbereik en hoogspannings waterige MXene planaire micro-supercondensatoren

 Welke van de volgende uitspraken suggereert relatieve leeftijd een toplaagsedimentaire rots zo oud daaronder B de aarde werd 4,6 miljard jaar geleden gevormd?
Welke van de volgende uitspraken suggereert relatieve leeftijd een toplaagsedimentaire rots zo oud daaronder B de aarde werd 4,6 miljard jaar geleden gevormd?  Wat is het moment van traagheidsfeer over de diameter van zijn diameter?
Wat is het moment van traagheidsfeer over de diameter van zijn diameter?  Exstinct Volcano Crater in de buurt van Napels die ooit als de ingang van de hel worden beschouwd?
Exstinct Volcano Crater in de buurt van Napels die ooit als de ingang van de hel worden beschouwd?  Fotosynthese:hoe organismen koolstof uit de omgeving verkrijgen
Fotosynthese:hoe organismen koolstof uit de omgeving verkrijgen  Wat is een hyopthese?
Wat is een hyopthese?  Wat is het verband tussen kinetische energie en beweging van deeltjes in een stof?
Wat is het verband tussen kinetische energie en beweging van deeltjes in een stof?  Milieuherstel na bosbranden:burgerwetenschappers leggen duizenden waarnemingen vast
Milieuherstel na bosbranden:burgerwetenschappers leggen duizenden waarnemingen vast Wat is de wetenschappelijke term voor waterliefde?
Wat is de wetenschappelijke term voor waterliefde?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

