
Wetenschap
De impact van waterstofionen op de menselijke gezondheid:hoe pH ons lichaam vormt
Door John Brennan
Bijgewerkt op 30 augustus 2022
ballero/iStock/GettyImages
Wanneer een Bronsted-zuur oplost in water, komen er waterstofionen (H⁺) vrij, waardoor de waterstofionenconcentratie van de oplossing stijgt. Chemici drukken deze concentratie uit als pH:hoe lager de pH-waarde, hoe hoger de dichtheid van waterstofionen. De pH-schaal varieert van 0 (sterk zuur) tot 14 (sterk alkalisch), waarbij 7 neutraliteit vertegenwoordigt. In het menselijk lichaam is een nauwkeurige pH-regeling essentieel voor tal van fysiologische processen.
TL;DR
Waterstofionen zijn de bouwstenen van de pH-schaal, die 0–14 beslaat. In waterige oplossingen bindt vrije H⁺ snel aan water om hydronium (H₃O⁺) te vormen. Het lichaam handhaaft de pH om de eiwitstructuur te behouden, spijsverteringsreacties te stimuleren en het zuurstoftransport in het bloed te reguleren.
De pH-schaal uitgelegd
In water bestaan geen geïsoleerde waterstofionen; ze associëren zich onmiddellijk met H₂O en creëren hydroniumionen (H₃O⁺). Bijgevolg weerspiegelt de pH de concentratie hydronium in plaats van vrij H⁺. Een pH van 7 duidt op een gelijke concentratie van H⁺- en hydroxide- (OH⁻)-ionen, terwijl pH-waarden dichter bij 0 een hoge concentratie waterstofionen aangeven en pH-waarden dichter bij 14 een lage concentratie aangeven.
Eiwitten en hun afhankelijkheid van de pH
Eiwitten zijn afhankelijk van waterstofbruggen tussen aminozuren om hun driedimensionale vorm te behouden. Variaties in de concentratie waterstofionen kunnen deze bindingen veranderen, waardoor eiwitten verkeerd vouwen of hun functie verliezen. Om dergelijke verstoringen te voorkomen, maken cellen gebruik van buffersystemen en gecompartimenteerde pH-regeling. Lysosomen houden bijvoorbeeld een lage pH-waarde aan om de afbraak van celafval te vergemakkelijken.
Maagzuur en spijsvertering
Pariëtale cellen langs de maag scheiden H⁺ en Cl⁻ af, die samen zoutzuur (HCl) vormen. Dit zuur verlaagt de pH van de maag tot ongeveer 1 à 2, waardoor de ingenomen bacteriën worden gedood en het enzym pepsine wordt geactiveerd. De optimale activiteit van pepsine vereist een specifieke waterstofionenomgeving, waardoor het voedingseiwitten in peptiden kan splitsen. Wanneer de maagbrij de maag verlaat, neutraliseert pancreasbicarbonaat het zuur, waardoor het darmslijmvlies wordt beschermd.
Bloed-pH en ademhalingsregulatie
De pH van het bloed wordt strak tussen 7,2 en 7,4 gehouden. Bij cellulaire ademhaling ontstaat CO₂, dat met water reageert en koolzuur genereert, waardoor de concentratie waterstofionen enigszins stijgt. Deze bescheiden zuurgraad zorgt ervoor dat hemoglobine zuurstof aan de weefsels afgeeft. Hemoglobine bindt vervolgens CO₂ en H⁺ voor transport terug naar de longen, waar lagere CO₂-niveaus de diffusie uit het bloed verdrijven, waardoor de pH van het bloed stijgt en de zuurstofopname wordt verbeterd.
Door te begrijpen hoe waterstofionen de pH beïnvloeden, krijgen we inzicht in het delicate evenwicht dat het leven in stand houdt.
Hoofdlijnen
- Wie zijn de twee wetenschappers die de ontwikkelingstheorie van evolutie door natuurlijke selectie hebben gecrediteerd?
- Wat is een recombinant enzym?
- Moet de wetenschappelijke methode in orde gaan, zo ja, waarom?
- Wat is de functie van gewas in een duif?
- Bloedmonsters tonen aan dat dodelijke kikkerschimmel in het wild aan het werk is
- Wat zijn de organisatieniveaus in anatomie en fysiologie?
- Hoe worden Saccos gevormd?
- Onderzoekers rapporteren een fundamentele spiersnelheidslimiet
- Wiskundige modellen laten zien waarom dieren 's nachts zien
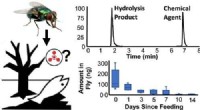
- Blaasvliegen kunnen worden gebruikt om het gebruik van chemische wapens en andere verontreinigende stoffen te detecteren
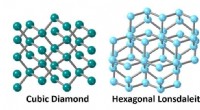
- We hebben in minuten zonder hitte diamanten gemaakt door de kracht van een asteroïdebotsing na te bootsen
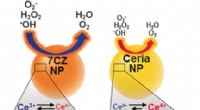
- Ceria-zirconia-nanodeeltjes als verbeterde multi-antioxidanten zijn effectief bij de behandeling van sepsis
- Ingenieurs melden een nieuwe methode voor het produceren van nieuwe flexibele LCD-schermen

- Onderzoek onthult mogelijke duurzame raffinagemethode voor lignine

 Welk model doen wetenschappers om atomen te bestuderen?
Welk model doen wetenschappers om atomen te bestuderen?  Hoe krijg je elektriciteit uit de zon?
Hoe krijg je elektriciteit uit de zon?  Evenveel noodtoestandverklaringen tijdens de eerste golf van de pandemie als in het voorgaande decennium
Evenveel noodtoestandverklaringen tijdens de eerste golf van de pandemie als in het voorgaande decennium Is meestal een gas- of brosse vaste stof die een slechte geleider van elektriciteit is?
Is meestal een gas- of brosse vaste stof die een slechte geleider van elektriciteit is?  Een nieuwe rol voor de eiwitfamilie zou een pad kunnen bieden voor de manier waarop gewaseigenschappen worden gewijzigd
Een nieuwe rol voor de eiwitfamilie zou een pad kunnen bieden voor de manier waarop gewaseigenschappen worden gewijzigd  Wat is een byproduct van smelterij?
Wat is een byproduct van smelterij?  Onderzoekers verbeteren de productie van textielcomposiet
Onderzoekers verbeteren de productie van textielcomposiet Kunnen door onbekende ambachtslieden individuele verschillen worden gedetecteerd in potten van hetzelfde gevormde aardewerk?
Kunnen door onbekende ambachtslieden individuele verschillen worden gedetecteerd in potten van hetzelfde gevormde aardewerk?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


