
Wetenschap
Atomen begrijpen:protonen, neutronen, elektronen en hun rollen
Door Kevin Beck
Bijgewerkt op 30 augustus 2022
Creatas/Creatas/Getty Images
Het atoom, afgeleid van het Griekse woord dat 'dat wat niet kan worden verdeeld' betekent, is de fundamentele eenheid van alle materie. Het is samengesteld uit subatomaire deeltjes:protonen, neutronen en elektronen. De protonen en neutronen bevinden zich in de kern en zijn verantwoordelijk voor bijna de gehele massa van het atoom, terwijl elektronen orbitalen aan de periferie bezetten.
Het proton
Protonen zijn de bepalende deeltjes van een element. Het aantal protonen (atoomnummer Z) identificeert elk element op unieke wijze. Waterstof heeft één proton (Z=1), het lichtste element, terwijl uranium 92 protonen heeft (Z=92), het zwaarste natuurlijk voorkomende element. Elk proton heeft een massa van 1,00728 atomaire massa-eenheden (amu) en heeft een lading van +1. Een kern die slechts één proton bevat, zoals die van waterstof, kwalificeert nog steeds als een atoom.
Het neutron
Neutronen, bijna even groot als protonen, hebben een massa van 1,00867amu en hebben geen elektrische lading. Het aantal neutronen in een kern varieert en overschrijdt doorgaans het aantal protonen, vooral voor zwaardere elementen. Een waterstofatoom heeft bijvoorbeeld één proton en geen neutronen; helium heeft twee protonen en twee neutronen; tin heeft 50 protonen en 69 neutronen; uranium heeft 92 protonen en 146 neutronen. De som van protonen en neutronen geeft het massagetal M. Het aantal neutronen is dus gelijk aan M − Z. Het veranderen van het neutronennummer levert isotopen op:atomen van hetzelfde element met verschillende massagetallen, bijvoorbeeld aangegeven als ¹⁴C voor koolstof met acht neutronen.
Het Elektron
Elektronen zijn minuscule, negatief geladen deeltjes met een massa van 0,000549amu. Ze draaien rond de kern in discrete energieniveaus (s-, p-, d- en f-orbitalen) in plaats van eenvoudige planetaire paden te volgen. In een neutraal atoom is het aantal elektronen gelijk aan het aantal protonen (Z), waardoor de algehele ladingsneutraliteit wordt gegarandeerd. Wanneer de getallen verschillen, wordt het atoom een ion, met een netto positieve of negatieve lading.
Het Atoom
Atomen zijn buitengewoon klein en met gewone middelen ondeelbaar, analoog aan de puzzelstukjes waaruit een legpuzzel bestaat. Hun structuur – protonen (positief), neutronen (neutraal) en elektronen (negatief) – bepaalt de eigenschappen van het element. Omdat elektronen vrijwel massaloos zijn vergeleken met protonen en neutronen, is de atoommassa feitelijk de som van protonen en neutronen.
 Het aantal verschillende elementen in de chemische formule van minerale scapoliet na2ca2al3si9o24cl?
Het aantal verschillende elementen in de chemische formule van minerale scapoliet na2ca2al3si9o24cl?  Emissies van verhitte tabaksproducten onderzoeken
Emissies van verhitte tabaksproducten onderzoeken Een nieuwe syntheseroute voor alternatieve katalysatoren van edelmetalen
Een nieuwe syntheseroute voor alternatieve katalysatoren van edelmetalen Inktvishuid inspireert tot het maken van een ruimtedeken van de volgende generatie
Inktvishuid inspireert tot het maken van een ruimtedeken van de volgende generatie Wat zijn de drie jodiumverbindingen?
Wat zijn de drie jodiumverbindingen?
 Lekken zullen de afvang en opslag van koolstof niet doen zinken
Lekken zullen de afvang en opslag van koolstof niet doen zinken 3D Grassland School Projects
3D Grassland School Projects Hoe maak je waterkwesties belangrijk voor wereldleiders
Hoe maak je waterkwesties belangrijk voor wereldleiders Wiens ideeën over materie leek het meest op wat wetenschappers vandaag gebruikten?
Wiens ideeën over materie leek het meest op wat wetenschappers vandaag gebruikten?  Koraalriffen voorkomen meer dan $ 5,3 miljard aan potentiële schade door overstromingen voor eigenaren van onroerend goed in de VS
Koraalriffen voorkomen meer dan $ 5,3 miljard aan potentiële schade door overstromingen voor eigenaren van onroerend goed in de VS
Hoofdlijnen
- Wat voor soort informatie wordt gepresenteerd door een wetenschapper die reden heeft om een bepaalde manier te presenteren?
- Wat moet een cel eerst doen om succesvol te verdelen?
- Fruitvliegjes laten zien hoe salmonella aan de immuunafweer ontsnapt
- Wat wordt er gevormd uit de eierstok?
- Infecties begrijpen:micro-organismen en virussen in het lichaam
- Wat is gebruikelijk in de structuur van alle cellen?
- Wie heeft de basis van de wetenschap van genetica vastgelegd?
- Wat zijn twee levende delen van een ecosysteem?
- Hoeveel soorten ribosomen zijn er?
- Protocell-gasten ontvluchten het nest

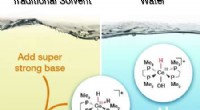
- Water verandert hoe een op kobalt gebaseerd molecuul koolstofdioxide omzet in een veelbelovende chemische stof
- Verfijning van thermo-elektrische materialen voor goedkopere hernieuwbare energie

- Hardnekkige biofilms wegspoelen met reinigingsproducten voor schimmels
- Nieuw begrip van hoe cellen tunnels vormen, kan helpen bij het behandelen van wonden, tumoren

 2015-2016 El Nino veroorzaakte ziekte-uitbraken over de hele wereld
2015-2016 El Nino veroorzaakte ziekte-uitbraken over de hele wereld De grote les uit eerdere pandemieën? Vermijd paniekaankopen, zegt nieuw onderzoek
De grote les uit eerdere pandemieën? Vermijd paniekaankopen, zegt nieuw onderzoek  Hoe verandert de dichtheid van de aarde met diepte?
Hoe verandert de dichtheid van de aarde met diepte?  Wat zijn de theorieën die de vorming van het zonnestelsel verklaren?
Wat zijn de theorieën die de vorming van het zonnestelsel verklaren?  Welke invloed op het klimaat?
Welke invloed op het klimaat?  Hoe werken hitte en interne energieverbruik?
Hoe werken hitte en interne energieverbruik?  Principes van galvaniseren
Principes van galvaniseren New Jerseys Pinelands zijn rijp voor een wildvuur van het Australische type
New Jerseys Pinelands zijn rijp voor een wildvuur van het Australische type
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

