
Wetenschap
De rol van buffers bij elektroforese:waarom ze essentieel zijn
Door Pete Collins | Bijgewerkt op 30 augustus 2022
TL;DR
Elektroforese scheidt macromoleculen zoals eiwitten en nucleïnezuren op grootte, lading en andere fysisch-chemische eigenschappen. Bij op lading gebaseerde scheidingen brengt een bufferoplossing het elektrische veld over en handhaaft een stabiele pH, waardoor de oorspronkelijke lading en structuur van de analyten behouden blijven. Deze stabiliteit is van cruciaal belang voor een nauwkeurige resolutie.
Principes van elektroforese
Elektroforese maakt gebruik van een aangelegd elektrisch veld (of een chemische gradiënt in gespecialiseerde technieken) om geladen moleculen door een gelmatrix te bewegen. Moleculen migreren naar de elektrode met tegengestelde lading:negatief geladen soorten reizen naar de anode, positief geladen soorten naar de kathode. Omdat grotere moleculen meer wrijving ervaren in de gel, bewegen ze langzamer dan kleinere, waardoor scheiding op basis van grootte mogelijk is. De gemigreerde afstand kan op een logaritmische schaal worden uitgezet om het molecuulgewicht of de fragmentlengte te schatten.
Denaturerende gradiëntgelelektroforese (DGGE)
DGGE introduceert een denaturerende gradiënt – doorgaans een mengsel van ureum en formamide – in de gel. Terwijl DNA-fragmenten de gradiënt doorkruisen, destabiliseren toenemende concentraties van denaturant geleidelijk de dubbele helix. Elk fragment stopt met migreren zodra de lokale concentratie van het denatureringsmiddel zijn smeltpunt bereikt. Deze techniek maakt gebruik van sequentie-afhankelijk smeltgedrag om DNA-fragmenten van identieke lengte maar met een verschillende sequentie op te lossen.
Wat de buffer doet
Bij op lading gebaseerde elektroforese geleiden de ionische soorten van de buffer het aangelegde elektrische veld door de gel, waardoor een uniforme stroomverdeling wordt gegarandeerd. Tegelijkertijd handhaaft het zwakke zuur-basepaar van de buffer de pH binnen een smal venster. Omdat de ladingstoestand en de driedimensionale structuur van eiwitten en nucleïnezuren pH-afhankelijk zijn, voorkomt een stabiele pH onbedoelde conformationele veranderingen die de scheidingsgetrouwheid in gevaar zouden kunnen brengen.
Typische buffers
Het kiezen van de juiste buffer hangt af van het gewenste pH-bereik en de noodzaak om de ionensterkte te minimaliseren, die anders overmatige hitte en vervorming zou kunnen veroorzaken. Veelgebruikte buffers zijn onder meer:
- Azijnzuur (pKa 4,76) – ideaal voor scheidingen met een lage pH.
- Boorzuur (pKa 9,24) – vaak gebruikt in op DNA gebaseerde tests.
- Fosforzuur (pKa 2,15, 7,20, 12,32) – veelzijdig voor een breed pH-spectrum.
- Citroenzuur (pKa 3,13, 4,76, 5,49) – zorgt voor buffering in het pH-bereik van 3–6.
- Glycine (pKa 2,34, 9,60) – gebruikelijk in Tris-glycinesystemen.
- Taurine (pKa 1,71) – gebruikt in gespecialiseerde elektroforetische protocollen.
Voor optimale prestaties moet de pKa van de buffer dicht bij de doel-pH liggen en moet de algehele ionensterkte laag genoeg zijn om de door stroom veroorzaakte opwarming te beperken, terwijl toch een efficiënte ladingsoverdracht mogelijk is.
Door zorgvuldig bufferomstandigheden te selecteren en te behouden, kunnen onderzoekers reproduceerbare scheidingen met hoge resolutie bereiken die essentieel zijn voor downstream-analyses.
 Hoe helpt wetenschap mensen te beslissen of huizen in een bepaald gebied moeten worden gebouwd?
Hoe helpt wetenschap mensen te beslissen of huizen in een bepaald gebied moeten worden gebouwd?  Afbeelding:NASA's Aqua-satelliet legt rook vast die voor de kust van Californië opstookt
Afbeelding:NASA's Aqua-satelliet legt rook vast die voor de kust van Californië opstookt Kanarie in de mijnwaarschuwing na nieuwe ontdekking van de effecten van verontreinigende stoffen op de vruchtbaarheid
Kanarie in de mijnwaarschuwing na nieuwe ontdekking van de effecten van verontreinigende stoffen op de vruchtbaarheid Wat is het verschil tussen bos uit struikgewas?
Wat is het verschil tussen bos uit struikgewas?  Verlaagd zwavelgehalte in scheepsbrandstof in verband met verhoogde maritieme opwarming van de atmosfeer
Verlaagd zwavelgehalte in scheepsbrandstof in verband met verhoogde maritieme opwarming van de atmosfeer
Hoofdlijnen
- Wat is de grootste organel in een cel?
- Waarom is het belangrijk om een bacteriecultuur te starten met een enkele geïsoleerde kolonie?
- Waarom vleermuizen niet ziek worden van de dodelijke ziekten die ze met zich meedragen
- Wat is de naam van de plaats waar voedingsstoffen bloed binnenkomen?
- Menselijke invloed op de evolutie:soorten en eigenschappen veranderen
- Wat betekent het woordklasse in een wetenschappelijke term?
- Steur blijft zeldzaam in de Grote Meren, maar de bevolking van Detroit Rivers bloeit
- Wat is het menselijke skeletsysteem?
- Wanneer de cel natrium van binnenuit uitschiet tegen de natuurlijke neiging van materie die het uitvoert.
- Activering van prodrug met behulp van in eiwit omhulde goudkatalysator
- Wetenschappers maken gigantische moleculaire kooien voor energieconversie en medicijnafgifte

- Kijken naar een toekomst waarin het ontdooien van vliegtuigen tot het verleden behoort

- Beeldvorming van chemische kinetiek op vloeistof-vloeistof-interfaces
- Onderzoekers ontwikkelen een viscositeitsmeettechniek voor zowel vloeistoffen als gassen
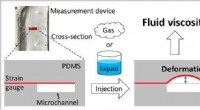
 Wat is de wetenschappelijke classificatie van spinazie?
Wat is de wetenschappelijke classificatie van spinazie?  Stamcellen van volwassen konijnen vertonen goede mogelijkheden voor laboratoriumgebruik
Stamcellen van volwassen konijnen vertonen goede mogelijkheden voor laboratoriumgebruik  Hoe verhoudt geologie zich tot de menselijke ervaring?
Hoe verhoudt geologie zich tot de menselijke ervaring?  Noem de 2 staten met een stad genaamd Noordpool?
Noem de 2 staten met een stad genaamd Noordpool?  Natriumbisulfaat in waterbehandeling:gebruik en voordelen
Natriumbisulfaat in waterbehandeling:gebruik en voordelen  Google-Fitbit-deal kan gegevens- en privacyrisico's met zich meebrengen, EU-privacyagentschap zegt:
Google-Fitbit-deal kan gegevens- en privacyrisico's met zich meebrengen, EU-privacyagentschap zegt: Deeltjesdetector bij Fermilab speelt cruciale rol in Deep Underground Neutrino Experiment
Deeltjesdetector bij Fermilab speelt cruciale rol in Deep Underground Neutrino Experiment Ontdekken van de akoestische eigenschappen van Stonehenge
Ontdekken van de akoestische eigenschappen van Stonehenge
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

