
Wetenschap
Hoe katalysatoren chemische reacties versnellen:een duidelijke gids
Rawpixel/iStock/GettyImages
Wanneer je wasmiddel gebruikt om een vlek op een overhemd te verwijderen, zie je een katalysator in actie tijdens een chemische reactie. Wasmiddelen bevatten enzymen, dit zijn katalysatoren die vuil en andere vlekken op kleding afbreken. Hoewel ze helpen de favoriete outfits van mensen schoon te maken, zijn ze niet de enige voorbeelden van krachtige katalysatoren.
TL;DR (te lang; niet gelezen)
Een katalysator versnelt een chemische reactie. De katalysator blijft na de reactie onveranderd.
Het effect van een katalysator op een chemische reactie
Het effect van een katalysator op een chemische reactie
Een katalysator beïnvloedt een chemische reactie door deze te versnellen. Het biedt ook een alternatieve manier om de reactie te laten plaatsvinden, waardoor de benodigde hoeveelheid energie wordt verlaagd. Reacties vereisen activeringsenergie om te starten, en katalysatoren kunnen daarbij helpen. Katalysatoren overleven de reacties echter onveranderd.
Twee manieren waarop katalysatoren een chemische reactie beïnvloeden
Twee manieren waarop katalysatoren een chemische reactie beïnvloeden
De twee belangrijkste manieren waarop katalysatoren chemische reacties beïnvloeden, zijn door een manier te creëren om de activeringsenergie te verlagen of door de manier waarop de reactie plaatsvindt te veranderen. Ze kunnen de energie van de overgangstoestand verlagen, zodat de totale activeringsenergie die nodig is voor de reactie afneemt, of ze kunnen de mechanismen van een reactie veranderen en zo de overgangstoestand veranderen.
Katalysatoren doen hun werk op verschillende manieren. Eén optie is dat deze stoffen de reactantmoleculen hun bindingen laten verbreken en nieuwe vormen met de katalysatoren. Deze bindingen zijn niet permanent, dus de katalysatoren kunnen de reacties onveranderd overleven. Een andere manier waarop katalysatoren werken is door de configuratie van de reactanten te veranderen en hun bindingen te verzwakken.
Voorbeelden van katalysatoren in chemische reacties
Voorbeelden van katalysatoren in chemische reacties
Twee soorten katalysatoren zijn homogeen en heterogeen. Homogene katalysatoren bevinden zich in dezelfde fase als de reactanten in de chemische reactie. Als de reactanten bijvoorbeeld gassen zijn, is de katalysator ook een gas. Heterogene katalysatoren bevinden zich in een andere fase dan de reactanten. De reactanten kunnen bijvoorbeeld vast zijn, maar de katalysator is een vloeistof.
Enzymen zijn een typisch voorbeeld van een biologische katalysator. Deze eiwitten kunnen op verschillende manieren vouwen om reacties te helpen door reactanten te binden. Katalysatoren kunnen helpen bij het hydrolyseren van sucrose of tafelsuiker. Invertase is een enzym dat helpt bij de afbraak van sucrose:sucrose + H2O levert glucose + fructose op.
Katalysatoren in auto's zijn een ander veelvoorkomend voorbeeld van hoe katalysatoren werken. De katalysatoren in de converters zijn meestal edelmetalen zoals platina of rhodium. Gassen komen de converter binnen en komen in contact met de katalysatoren. Vervolgens reageren schadelijke verontreinigende stoffen met de metalen en worden ze minder giftig.
 Wetenschappers ontdekken groenere route naar veelgebruikt industrieel materiaal
Wetenschappers ontdekken groenere route naar veelgebruikt industrieel materiaal Gevonden:een nauwkeurige methode om te bepalen hoe golven en deeltjes fusiereacties beïnvloeden
Gevonden:een nauwkeurige methode om te bepalen hoe golven en deeltjes fusiereacties beïnvloeden  Zes elementen genoemd naar wetenschappers
Zes elementen genoemd naar wetenschappers Metaalschuim kan geluid onder hoge druk absorberen, omgevingen met hoge temperaturen zoals straalmotoren
Metaalschuim kan geluid onder hoge druk absorberen, omgevingen met hoge temperaturen zoals straalmotoren Hoe zijn zowel gassen als vloeistoffen?
Hoe zijn zowel gassen als vloeistoffen?
Hoofdlijnen
- Hoe herstelt de huid?
- Wat zijn de twee functies van eiwitten?
- Voorbereiden op toekomstige coronavirusvarianten met behulp van kunstmatige intelligentie
- Welke planten zonder tubelike cellen moeten altijd in de buurt hebben?
- Hoe is een levend wezen dat een ander produceert zoals hij wordt genoemd?
- Welke structuren hebben bacteriën XY?
- Het gebruik van van bacteriofaag afkomstige lysine om geurveroorzakende bacteriën in oksels aan te pakken
- Waarom moet het immuunsysteem pathogeen vernietigen?
- Hoeveel krijgt een wetenschapper betaald door de biologie?
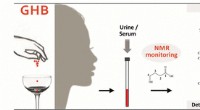
- De detectie van een date rape drug verbeteren
- Haast om medicijnen te ontwikkelen? Hier is je chat
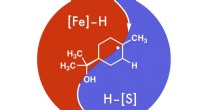
- Nanomateriaal vernietigt zenuwgassen in omstandigheden die relevant zijn voor het slagveld

- Synthetisch gelatineachtig materiaal bootst de rek en sterkte van de onderbuik van kreeft na
- Doorbraak in elektrolyse kan het waterstofvraagstuk oplossen

 Wat is zwaartekrachtsnelheid of snelheid?
Wat is zwaartekrachtsnelheid of snelheid?  Eerste directe bewijs van oceaanvermenging over de Golfstroom
Eerste directe bewijs van oceaanvermenging over de Golfstroom Overstromingen door overblijfselen van tropische stormen vangen Phoenix-auto's op
Overstromingen door overblijfselen van tropische stormen vangen Phoenix-auto's op Ongeveer 90 procent van de sterren op Hertzsprung-Rusell-diagram zijn?
Ongeveer 90 procent van de sterren op Hertzsprung-Rusell-diagram zijn?  Worm Snakes in Georgia
Worm Snakes in Georgia  Hevige regenval orkaan Michaels gemeten door NASA
Hevige regenval orkaan Michaels gemeten door NASA Wat is een verweerde rots?
Wat is een verweerde rots?  Hoe berekenen elektrische bedrijven de gebruikte energie?
Hoe berekenen elektrische bedrijven de gebruikte energie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

