Wetenschap
Het behoud van massa:hoe het balanceren van chemische vergelijkingen een fundamentele wet aantoont
DragonImages/iStock/GettyImages
Behoud van de massa:de fundamentele wet
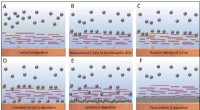
Het behoud van massa houdt in dat de totale massa in een gesloten systeem constant blijft:er kan tijdens een chemische reactie geen materie ontstaan of vernietigd worden. In de praktijk is de som van de massa's van reactanten gelijk aan de som van de massa's van producten, en is het totale aantal atomen voor elk element identiek aan beide kanten van de vergelijking.
Historische wortels
In 1789 formaliseerde Antoine Lavoisier het principe na nauwgezette experimenten, waardoor het een hoeksteen van de moderne chemie werd. Hoewel eerdere Griekse filosofen zoals Anaxagoras opmerkten dat materie alleen maar wordt herschikt, leverde Lavoisiers kwantitatieve werk hem de eer op voor het ontdekken van de wet.
Praktische stappen voor het balanceren van vergelijkingen
1. Tel de atomen van elk element aan beide kanten.
2. Als de aantallen verschillen, introduceer dan gehele coëfficiënten vóór de molecuulformules. De coëfficiënten moeten hele getallen zijn en mogen de chemische formules niet veranderen.
3. Pas de coëfficiënten iteratief aan totdat elk element in evenwicht is.
Voorbeeld:ammoniaksynthese
Ongebalanceerd:N₂ + H₂ → NH₃
Balanceringsproces:Voeg een coëfficiënt van 3 toe aan H₂ en 2 aan NH₃ om N₂ + 3H₂ → 2NH₃ te bereiken . Elk element verschijnt nu aan beide kanten in gelijke aantallen.
Ga voor meer details naar Wikipedia:Behoud van massa .
 Fysische en gedragsaanpassing van Skunks
Fysische en gedragsaanpassing van Skunks Krachtige tyfoon Faxai teistert de regio Tokio
Krachtige tyfoon Faxai teistert de regio Tokio Wat is het abstracte zelfstandig naamwoord voor zuur?
Wat is het abstracte zelfstandig naamwoord voor zuur?  Asteroïde, klimaatverandering niet verantwoordelijk voor massale uitsterving 215 miljoen jaar geleden
Asteroïde, klimaatverandering niet verantwoordelijk voor massale uitsterving 215 miljoen jaar geleden Wie boom heeft het blad dat in de ochtend witte middag rood en avondgroene nacht zwart?
Wie boom heeft het blad dat in de ochtend witte middag rood en avondgroene nacht zwart?
Hoofdlijnen
- Zijn eiwitten gevonden in het celmembraan?
- Een structuur in eukaryotische cellen die werkt als een gespecialiseerd orgaan?
- Een praktische gids voor het ontwerpen van PCR-primers
- Hoe zijn enzymen belangrijk voor chemische reacties in cellen?
- Onderzoek laat zien hoe landbouwgronden de verspreiding van bijenziekten beïnvloeden
- Waarom beschouwen auteurs syndesmosis als een voorbeeld van amfiarthrose?
- Welke organel regelt de activiteiten van plantencel?
- Overbevissing:Is er echt veel vis in de zee?
- Is het mogelijk om een knock -out mutantplant te hebben die geen zichtbaar fenotype vertoont, verschilt van de wildtype plant?
 Amerikaanse centrale bank gaat virtuele valuta van Facebook bestuderen
Amerikaanse centrale bank gaat virtuele valuta van Facebook bestuderen Wat gebeurt er als een positief geladen dirigent is geaard?
Wat gebeurt er als een positief geladen dirigent is geaard?  Hoe koolstof in de bodem kan helpen de klimaatverandering aan te pakken
Hoe koolstof in de bodem kan helpen de klimaatverandering aan te pakken Zware metalen uit water verwijderen met MOF's
Zware metalen uit water verwijderen met MOF's Welke energietransformatie vindt plaats in een zonne -calculator?
Welke energietransformatie vindt plaats in een zonne -calculator?  Wat is oscillerende beweging?
Wat is oscillerende beweging?  Welke massa zuurstof bevat hetzelfde aantal moleculen als 42 g stikstof?
Welke massa zuurstof bevat hetzelfde aantal moleculen als 42 g stikstof?  Wat Spotify en Tinder ons niet vertellen
Wat Spotify en Tinder ons niet vertellen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com