
Wetenschap
Vier soorten orbitalen en hun vormen – een praktische gids
Door Richard Gaughan Bijgewerkt op 30 augustus 2022
twilightproductions/iStock/GettyImages
Atomen bestaan uit een zware kern omgeven door lichte elektronen. De kwantummechanica dicteert dat elektronen verschillende gebieden bezetten die orbitalen worden genoemd. Omdat chemische interacties voornamelijk plaatsvinden via de buitenste elektronen, is de vorm van deze orbitalen cruciaal om te begrijpen hoe atomen zich binden en zich gedragen.
Kwantumgetallen en orbitalen
Natuurkundigen beschrijven de toestand van een elektron met een reeks gehele kwantumgetallen. Het hoofdkwantumgetal n heeft betrekking op energie, terwijl het orbitale kwantumgetal l en het magnetische kwantumgetal m bepaal de geometrie en oriëntatie van de orbitaal. Er bestaan nog meer kwantumgetallen, maar deze hebben geen directe invloed op de orbitale vorm. Orbitalen vertegenwoordigen waarschijnlijkheidswolken (geen letterlijke elektronenpaden) rond de kern.
S-orbitalen
Voor elke waarde van n , is er één orbitaal waar beide l en m gelijk aan nul. Dit zijn bolvormige schelpen, die in omvang groter worden als n neemt toe. De s-orbitaal is het enige type dat bestaat voor de grondtoestand (n=1) en komt voor op elk hoofdenergieniveau. Hoewel de elektronendichtheid nabij de kern hoger is, is de bol feitelijk genest als concentrische schillen.
P-orbitalen
Wanneer n groter is dan één, ontstaan er extra orbitale typen. Voor l gelijk is aan één, wordt de orbitaal een p-orbitaal genoemd. Deze lijken op halters. Elke l waarde staat m toe variëren van –l naar +l in stappen van gehele getallen, wat drie p-orbitalen oplevert op elk niveau boven n=1:één georiënteerd langs de z-as (m=0) en twee orthogonaal in het x-y-vlak (m=±1). P-orbitalen verschijnen in alle belangrijke energieniveaus boven de eerste, met subtiele structurele veranderingen als n groeit.
D-orbitalen
Bij n=3, l kan 2 zijn, wat aanleiding geeft tot d-orbitalen. Er zijn vijf verschillende d-orbitalen die overeenkomen met m =–2, –1, 0, 1, 2. De m=0 d-orbitaal lijkt op een halter met een ringkern “donut” in het midden, terwijl de andere vier lijken op vier lobben die in een vierkante piramide zijn gerangschikt, elk anders georiënteerd. D-orbitalen zijn aanwezig wanneer het hoofdkwantumgetal minstens drie is.
F-orbitalen
Voor n=4, l is gelijk aan 3, wat f-orbitalen oplevert. Dit zijn de meest complexe en moeilijk te visualiseren. De m=0, ±1 orbitalen lijken op halters met twee toroïdale ringen die de centrale balk flankeren, terwijl de overige m-waarden vormen produceren die lijken op bundels van acht ballonnen die aan elkaar zijn vastgebonden in een centrale knoop. F-orbitalen komen beschikbaar op alle energieniveaus waarbij n vier of groter is.
Visualisaties
De wiskunde achter elektronenorbitalen is ingewikkeld, maar talloze online tools geven deze vormen grafisch weer. Dergelijke visualisaties zijn van onschatbare waarde om te begrijpen hoe elektronen zich rond een kern verdelen.
Hoofdlijnen
- Wetenschappers bieden nieuw inzicht in de manier waarop genexpressie wordt gecontroleerd
- Er wordt gezegd dat twee soorten nauw verwant zijn als zij?
- Wordt Lily groeit uit een bol?
- Wat is een stof die geen deel uitmaakt van een organismen van een organismen?
- Avocado's zijn 'slecht' en veganisten belachelijk:hoe we het eten van te veel vlees rechtvaardigen
- Van bijna uitsterven tot herstel:de opmerkelijke comeback van de zwartvoetfret
- Welk type organisch macromolecuul is glucose?
- De oorsprong van het leven in een RNA-pocket
- Hoe helpen eiwitten ons?
- Onderzoekers ontwikkelen nieuwe methoden om materialen op de kleinst mogelijke schaal te bestuderen

- Een hybride materiaal dat omkeerbaar schakelt tussen twee stabiele vaste toestanden
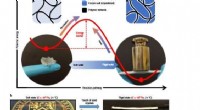
- De 3D-vorm van moleculen ontdekken met een druk op de knop
- Magnetische tanden onthuld met behulp van kwantumbeeldvorming

- Stimulatie van kleine gebieden op celoppervlakken met vrije radicalen met behulp van een microfluïdische sonde

 Beschrijf hoe eukaryoten zijn geëvolueerd?
Beschrijf hoe eukaryoten zijn geëvolueerd?  De nadelen van ontbossing
De nadelen van ontbossing  Als een reactie optreedt, wat zullen de producten van onevenwichtige ondermg (s) plus H2O (L) zijn?
Als een reactie optreedt, wat zullen de producten van onevenwichtige ondermg (s) plus H2O (L) zijn?  Stuurt de zon golf radiogolven uit?
Stuurt de zon golf radiogolven uit?  Leg het belang van chemie uit voor uw dagelijks leven en de samenleving?
Leg het belang van chemie uit voor uw dagelijks leven en de samenleving?  Welke van de volgende organismen missen een celwand?
Welke van de volgende organismen missen een celwand?  Wat is thermische energie op zonne -energie en hoe het werkt?
Wat is thermische energie op zonne -energie en hoe het werkt?  30 ml is gelijk aan hoeveel milligram?
30 ml is gelijk aan hoeveel milligram?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


