
Wetenschap
Berekening van de calorimeterwarmte (Qcal):een praktische gids
Door Sean Butner, bijgewerkt op 30 augustus 2022
De wet van Hess ondersteunt het behoud van energie bij chemische reacties en beweert dat de warmte die vrijkomt of wordt geabsorbeerd door een reactie gelijk is aan de som van de warmte van de samenstellende stappen ervan. Een calorimeter biedt een gesloten systeem om deze warmtestroom vast te leggen. Hoewel het instrument idealiter de werkelijke enthalpieverandering registreert, absorbeert het ook een meetbare hoeveelheid warmte. Door de warmtecapaciteit van de calorimeter (Qcal) te bepalen, kunnen we de ruwe meetwaarde corrigeren en de werkelijke warmteverandering van de reactie verkrijgen.
1. Bepaal de soortelijke warmte van de calorimeter (Ccal)
Stap 1
Pas een bekende warmtebron toe, zoals een bunsenbrander met een gekalibreerd vermogen (Watt), op de lege calorimeter.
Stap 2
Meet de tijd (seconden) die nodig is voordat de temperatuur van de calorimeter precies één graad Celsius stijgt.
Stap 3
Vermenigvuldig het vermogen (Watt) met de gemeten tijd (seconden). Het product levert Ccal op in joule per graad Celsius (J°C⁻¹).
2. Bereken Qcal voor een reactie
Stap 1
Noteer de temperatuurverandering (ΔT in °C) die optreedt tijdens de reactie in de calorimeter.
Stap 2
Vermenigvuldig de eerder bepaalde Ccal met ΔT. Als Ccal =3,5 J°C⁻¹ en de reactie de temperatuur van de calorimeter met 5°C verhoogt, is het product 17,5 J.
Stap 3
Qcal is gelijk aan dit product. Een positieve waarde geeft de warmte aan die door de calorimeter wordt geabsorbeerd, terwijl een negatieve waarde de vrijkomende warmte aangeeft. Neem Qcal op in de algehele energiebalans om de werkelijke reactie-enthalpie te verkrijgen.
 Waarom wordt natriummetaal opgeslagen in vloeibare paraffine?
Waarom wordt natriummetaal opgeslagen in vloeibare paraffine?  Wat zou de lading van zuurstof zijn als het ioniseert?
Wat zou de lading van zuurstof zijn als het ioniseert?  Hoe Nigeria zijn enorme cashewafval kan omzetten in waardevol citroenzuur
Hoe Nigeria zijn enorme cashewafval kan omzetten in waardevol citroenzuur  Natriumsulfaat:eigenschappen en vormen (vaste en waterige oplossing)
Natriumsulfaat:eigenschappen en vormen (vaste en waterige oplossing)  Wat is de chemische formule van diammoniumwaterstoffosfaat?
Wat is de chemische formule van diammoniumwaterstoffosfaat?
 Hoe twee wetenschappers het natuurlijke koolstofbudget van de planeet in evenwicht brengen
Hoe twee wetenschappers het natuurlijke koolstofbudget van de planeet in evenwicht brengen De vier elementen:vuur, water, aarde en lucht verkennen - welke is het sterkst?
De vier elementen:vuur, water, aarde en lucht verkennen - welke is het sterkst?  Tropische regenwoudplanten voor kinderen
Tropische regenwoudplanten voor kinderen Is de hechtingstheorie eigenlijk belangrijk voor romantische relaties?
Is de hechtingstheorie eigenlijk belangrijk voor romantische relaties?  Nieuw-Zeeland markeert verwoestende verjaardag van vulkaanuitbarsting
Nieuw-Zeeland markeert verwoestende verjaardag van vulkaanuitbarsting
Hoofdlijnen
- Wat is een keten van bacteriën die staaf vormt?
- Wat zijn 5 wetenschappers die hebben bijgedragen aan wat we nu weten over cellen en hun bijdragen uitleggen?
- Welke tak van de wetenschap is het menselijk geheugen?
- Wat is een neogene recombinator?
- Wat veroorzaakt een stressor binnen een organisme?
- De effecten van straling op dieren
- Welke kenmerken van alle organismen en virussen worden bepaald door de instructies die zijn uitgevoerd?
- Nucleïnezuren:structuur, functie en belang
- Wat voor soort wetenschapper bestudeert de interacties tussen levensvormen en milieu?
- Travelling-wave ion mobility massaspectrometrie verheldert structuren van gouden vingers
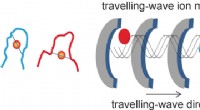
- De relatie tussen atmosferische druk en kookpunt uitgelegd

- Zelfherstellende folie op gelatinebasis kan een slimme zet zijn voor elektronica
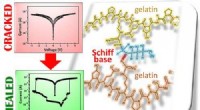
- Een betaalbare manier om schone energie op te slaan

- Sterke velden en ultrasnelle bewegingen - hoe elektronen in vloeibaar water te genereren en te sturen?
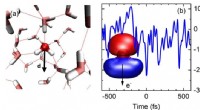
 Welk type cellen organiseert berichten in een menselijk lichaam?
Welk type cellen organiseert berichten in een menselijk lichaam?  Wat is de hoogste Mount Shasta om de dichtstbijzijnde voet te verklaren?
Wat is de hoogste Mount Shasta om de dichtstbijzijnde voet te verklaren?  Welke vier kenmerken van de geografie van Californië verklaart plaattektoniek?
Welke vier kenmerken van de geografie van Californië verklaart plaattektoniek?  Is opgeloste stof altijd in een solide vorm?
Is opgeloste stof altijd in een solide vorm?  Wat is een hulpmiddel dat magnetisch veld gebruikt om elektronen te focussen?
Wat is een hulpmiddel dat magnetisch veld gebruikt om elektronen te focussen?  Klimaatverandering:een veelbelovende toekomst voor katoen in Kameroen?
Klimaatverandering:een veelbelovende toekomst voor katoen in Kameroen?  Met extra suiker, bladeren worden ook dik
Met extra suiker, bladeren worden ook dik Hoeveel monochloroisomeren van cyclohexaan zijn mogelijk?
Hoeveel monochloroisomeren van cyclohexaan zijn mogelijk?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

