
Wetenschap
Theoretische opbrengst berekenen:een stapsgewijze handleiding in mol en gram
Door Emma Francesca • Bijgewerkt 30 augustus 2022
Bij een chemische reactie combineren reactanten in nauwkeurige stoichiometrische verhoudingen om producten te vormen. Onder ideale laboratoriumomstandigheden kunt u precies voorspellen hoeveel product er uit een bepaalde hoeveelheid reactant zal komen. Die voorspelde hoeveelheid wordt de theoretische opbrengst genoemd. Voor een nauwkeurige berekening ervan is het nodig dat u de hoeveelheden reactanten en producten kent die daadwerkelijk worden gebruikt, en dat u de beperkende reactant identificeert.
Stap 1 – Schrijf de gebalanceerde vergelijking
Begin met een correct uitgebalanceerde chemische vergelijking. Dit zorgt ervoor dat de molverhoudingen tussen reactanten en producten nauwkeurig zijn.
Stap 2 – Bepaal de molmassa's
Gebruik een betrouwbaar periodiek systeem om de atoomgewichten van alle atomen in elke soort bij elkaar op te tellen. Deze waarden zijn uw molmassa's.
Stap 3 – Identificeer stoichiometrische verhoudingen
Noteer uit de uitgebalanceerde vergelijking de molverhoudingen. Als 1 mol reactant A bijvoorbeeld 2 mol product B oplevert, is de verhouding 1:2.
Stap 4 – Vergelijk de werkelijke bedragen met de vergelijking
Als de hoeveelheden die u heeft overeenkomen met die in de uitgebalanceerde vergelijking, is de theoretische opbrengst gelijk aan de producthoeveelheid die in de vergelijking wordt weergegeven. Converteer die waarde naar grammen door het aantal mol te vermenigvuldigen met de molaire massa van het product.
Stap 5 – Converteer gram naar mol
Wanneer je begint met massa's in grammen, deel je deze door de molaire massa om het aantal mol te verkrijgen.
Stap 6 – Identificeer de beperkende reagens
Gebruik de stoichiometrische verhoudingen uit stap 3 en vergelijk de moedervlekken die u heeft (uit stap 5) met de benodigde moedervlekken. De reactant die als eerste opraakt, beperkt de reactie.
Stap 7 – Bereken het theoretische rendement
Pas de molverhouding toe tussen de beperkende reactant en het gewenste product. Als 2 mol van de beperkende reactant bijvoorbeeld 3 mol product oplevert, levert 1 mol van de beperkende reactant 1,5 mol product op.
Stap 8 – Converteer mol product naar gram
Vermenigvuldig het theoretische aantal mol product met de molaire massa om de opbrengst in grammen te verkrijgen.
TL;DR (te lang; niet gelezen)
Als bij een reactie één enkele reactant betrokken is, is die reactant automatisch de beperkende reactant.
Referenties
- "Chemie" – John Olmsted et al., 2006
 Hoe beïnvloedt het klimaat in Modoc bieregion de bodem?
Hoe beïnvloedt het klimaat in Modoc bieregion de bodem?  Penny wise en pound foolish? Het budget van NYC moet rekening houden met de onderlinge verbondenheid van de infrastructuur van de stad
Penny wise en pound foolish? Het budget van NYC moet rekening houden met de onderlinge verbondenheid van de infrastructuur van de stad Hoe heeft papier effect op de samenleving?
Hoe heeft papier effect op de samenleving?  Belastingen en limieten op koolstof werken anders, maar het kalibreren ervan vormt dezelfde uitdaging
Belastingen en limieten op koolstof werken anders, maar het kalibreren ervan vormt dezelfde uitdaging Ecologische complexiteit en de biosfeer:de komende 30 jaar
Ecologische complexiteit en de biosfeer:de komende 30 jaar
Hoofdlijnen
- Welke soorten cellen worden er uit meiose geproduceerd?
- Alle levende wezens bestaan uit kleine cellen.
- Wat maakt mensen menselijk?
- Wat is een sporofyt?
- Wat is de aard van de celwand in ColenchyMa?
- Welke reeks vertegenwoordigt de juiste volgorde van niveaus organisatie die in een complex organisme wordt gevonden?
- Wat maakt een plant een plant?
- Onderzoekers ontdekken hoe CRISPR/Cas vreemd DNA steelt voor het bacteriële immuunsysteem
- Wat zijn levende organismen die ziekten veroorzaken?
- Polyimidemembranen voor de zuivering van aardgas
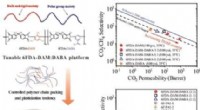
- Onderzoek naar een thermische uitdaging voor MOF's

- Moleculaire geheimen onthuld:antipsychoticum gedokt in zijn receptor
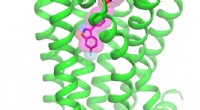
- De kern van hoe uien je aan het huilen maken
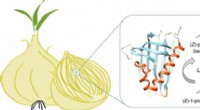
- Geschiedenis van inzichtelijk hiv-onderzoek inspireert neutronenverstrooiingsbenadering bij het bestuderen van COVID-19
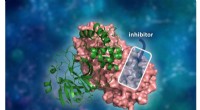
 Wie zei dat de planeet rond het zonnestelsel gaat?
Wie zei dat de planeet rond het zonnestelsel gaat?  Waarom concludeerden astronomen dat Pulsars geen pulserende sterren konden zijn?
Waarom concludeerden astronomen dat Pulsars geen pulserende sterren konden zijn?  Hoe gebruik je een schaduwklok?
Hoe gebruik je een schaduwklok?  Hoe Solar Insolation te berekenen
Hoe Solar Insolation te berekenen  Dodelijke moessonregenval in India gemeten met NASA's IMERG
Dodelijke moessonregenval in India gemeten met NASA's IMERG Hoe reguleert de autofagische route de stikstofarme tolerantie in tomaat?
Hoe reguleert de autofagische route de stikstofarme tolerantie in tomaat? Wat is de hypothese voor zetmeel?
Wat is de hypothese voor zetmeel?  Het verminderen van vallen verhoogt de prestaties van organische fotodetectoren
Het verminderen van vallen verhoogt de prestaties van organische fotodetectoren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

