
Wetenschap
Hoe Romeinse cijfers de metaaloxidatietoestanden in chemische verbindingen definiëren
Hemera Technologies/PhotoObjects.net/Getty Images
Metaalelementen vertonen vaak meerdere oxidatietoestanden, die de samenstelling van hun verbindingen bepalen. Hoewel de traditionele achtervoegsels "-ous"/"-ic" ooit gebruikelijk waren, geven scheikundigen nu de voorkeur aan het beknopte Romeinse cijfersysteem dat volgt op de naam van het metaal, en dat duidelijk de oxidatietoestand ervan aangeeft.
Koperchloriden
Koper kan twee chloridezouten vormen:CuCl en CuCl2 . In CuCl heeft het chloride-ion een lading van -1, waardoor koper +1 moet zijn. Deze verbinding wordt koper(I)chloride genoemd (koperchloride), een wit poeder dat wordt gebruikt in vuurwerk en als kleurstof. In CuCl2 geven twee chloride-ionen een totale lading van -2, dus koper is +2. Het resulterende zout is koper(II)chloride (koperchloride), blauwgroen indien gehydrateerd; het wordt gebruikt in vuurwerk, als katalysator en als pigment.
IJzeroxiden
De oxidatietoestanden van ijzer manifesteren zich in verschillende oxiden:
- FeO – één zuurstofion (-2) betekent dat ijzer +2 is, genaamd ijzer(II)oxide (ijzeroxide), overvloedig aanwezig in de aardmantel.
- Fe2 O3 – drie zuurstofionen (‑6) vereisen twee ijzerionen (+6 totaal), wat ijzer(III)oxide oplevert (ijzeroxide), beter bekend als roest.
- Fe3 O4 – vier zuurstofionen (‑8) worden in evenwicht gehouden door drie ijzerionen (+8 totaal) in een gemengde oxidatietoestand (+3 en +2), genaamd ijzer(II,III)oxide .
Tinchloriden
Tin neemt gewoonlijk +2 en +4 oxidatietoestanden aan:
- SnCl2 – twee chloride-ionen (‑2) vereisen tin +2, genaamd tin(II)chloride (stannochloride), een kleurloze vaste stof die wordt gebruikt bij het verven van textiel, galvaniseren en het bewaren van voedsel.
- SnCl4 – vier chloride-ionen (-4) vereisen tin +4, genaamd tin(IV)-chloride (stanninechloride), een kleurloze vloeistof bij kamertemperatuur.
Kwikbromiden
Kwik vormt twee bromidezouten:
- Hg2 Br2 – twee bromide-ionen (-2) splitsen zich tussen twee kwikatomen, waardoor elk een +1 oxidatietoestand krijgt. Dit is kwik(I)bromide (kwikbromide), gebruikt in akoestisch-optische apparaten.
- HgBr2 – een enkel kwikatoom met een +2 toestand brengt de twee bromide-ionen in evenwicht. Dit is kwik(II)bromide (kwikbromide), dat zeer giftig is.
 Hydronium- (H₃O⁺)- en hydroxide- (OH⁻)-concentraties in waterige oplossingen berekenen
Hydronium- (H₃O⁺)- en hydroxide- (OH⁻)-concentraties in waterige oplossingen berekenen  Welke elementen behoren tot de Nobelgassen?
Welke elementen behoren tot de Nobelgassen?  Welk element vertegenwoordigt een verbinding?
Welk element vertegenwoordigt een verbinding?  Welk chemisch proces verbindt monomeren samen?
Welk chemisch proces verbindt monomeren samen?  Supersmering op microschaal zou de weg kunnen effenen voor toekomstige verbeterde elektromechanische apparaten
Supersmering op microschaal zou de weg kunnen effenen voor toekomstige verbeterde elektromechanische apparaten
 Gestrande activa kunnen hoge kosten met zich meebrengen voor producenten en investeerders van fossiele energie
Gestrande activa kunnen hoge kosten met zich meebrengen voor producenten en investeerders van fossiele energie Welke drie dingen zijn ecologische piramides die worden gebruikt om te vertegenwoordigen?
Welke drie dingen zijn ecologische piramides die worden gebruikt om te vertegenwoordigen?  VS heeft de natste 12 maanden ooit - opnieuw
VS heeft de natste 12 maanden ooit - opnieuw Hoe verhoudt de wet van het behoud van behoud zich tot fotosynthese en ademhalingschemische vergelijkingen?
Hoe verhoudt de wet van het behoud van behoud zich tot fotosynthese en ademhalingschemische vergelijkingen?  Wat gebeurt er met een regenwoud als het wordt gekapt?
Wat gebeurt er met een regenwoud als het wordt gekapt?
Hoofdlijnen
- Welk type bloedcel is verantwoordelijk voor immuniteit?
- Welke twee dingen hebben wetenschappers geholpen meer details in cellen te zien?
- Wat moet u doen als u het defecte gen heeft?
- Wat wordt bedoeld met de stelling dat DNA alle organismen verenigt?
- Welke naam wordt gegeven aan de regio waar fotosynthese kan optreden?
- Wat zijn essentiële DNA -moleculen?
- Wat is de reactie van een basis met eiwitten?
- Waarom zijn blaasjes belangrijk in een cel?
- Wat is de toestand van een cel op het punt om mitose te starten?
- Zink reguleert de opslag en afgifte van neurotransmitters

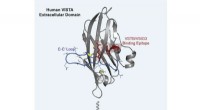
- Nieuw inzicht in een kankerbeschermend eiwit kan leiden tot een nieuwe generatie kankerbehandelingen
- Onderzoekers ontwerpen nieuw materiaal met behulp van kunstmatige intelligentie

- Gericht op verborgen zak voor behandeling van beroerte en epileptische aanvallen
- Overgangsmetaalcomplexen:gemengd werkt beter

 Waar strijden organismen volgens de evolutietheorie van Darwin om?
Waar strijden organismen volgens de evolutietheorie van Darwin om?  Hoe CERN-technieken voor machinaal leren autonome voertuigen kunnen verbeteren
Hoe CERN-technieken voor machinaal leren autonome voertuigen kunnen verbeteren Wat is een vorm van energie die door draden beweegt?
Wat is een vorm van energie die door draden beweegt?  Wanneer verliet de Apollo 11 de atmosfeer van de aarde?
Wanneer verliet de Apollo 11 de atmosfeer van de aarde?  Hoe ziet ethyleendiaminetetraaceticzuur eruit?
Hoe ziet ethyleendiaminetetraaceticzuur eruit?  Zeven morele regels gevonden over de hele wereld
Zeven morele regels gevonden over de hele wereld Energie kan nooit worden gecreëerd of vernietigd wat wat?
Energie kan nooit worden gecreëerd of vernietigd wat wat?  Waarom Mars Orbit Jupiter?
Waarom Mars Orbit Jupiter?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

