
Wetenschap
Isomeren begrijpen:waarom verbindingen empirische formules delen
Hier is een overzicht:
* Empirische formule: Toont de eenvoudigste verhouding van atomen in een verbinding.
* Moleculaire formule: Toont het werkelijke aantal van elk type atoom in een molecuul.
Voorbeeld:
* Glucose (C6H12O6) en Azijnzuur (C2H4O2) beide hebben dezelfde empirische formule:CH2O .
* Glucose heeft een molecuulformule van C6H12O6 , wat betekent dat het zes koolstofatomen, twaalf waterstofatomen en zes zuurstofatomen bevat.
* Azijnzuur heeft de molecuulformule C2H4O2 , wat betekent dat het twee koolstofatomen, vier waterstofatomen en twee zuurstofatomen bevat.
Waarom gebeurt dit?
Covalente verbindingen kunnen verschillende rangschikkingen van dezelfde atomen vormen, wat resulteert in verschillende structuren en eigenschappen. Deze verschillende arrangementen kunnen leiden tot verschillende molecuulformules, maar tot dezelfde empirische formule.
Samengevat:
De empirische formule geeft slechts een vereenvoudigd beeld van de samenstelling van de verbinding. Het toont niet het werkelijke aantal atomen in een molecuul, wat nodig is om onderscheid te maken tussen verschillende covalente verbindingen met dezelfde empirische formule.
 Wat gebeurt er bij het plaatsen van ijzeren nagels in een beker die kopersulfaat bevat?
Wat gebeurt er bij het plaatsen van ijzeren nagels in een beker die kopersulfaat bevat?  Hoe inerte verbindingen ionen kunnen stelen
Hoe inerte verbindingen ionen kunnen stelen Waar is de derde tanden in een gepolariseerd bakje dat voor wordt gebruikt?
Waar is de derde tanden in een gepolariseerd bakje dat voor wordt gebruikt?  Wat is de naam van hybride orbitalen die door zwavel in SCL2 worden gebruikt?
Wat is de naam van hybride orbitalen die door zwavel in SCL2 worden gebruikt?  Bereken het aantal moleculen in 9 g CO2?
Bereken het aantal moleculen in 9 g CO2?
 COVID-19-lockdown verminderde gevaarlijke luchtverontreinigende stoffen in vijf Indiase steden tot 54 procent
COVID-19-lockdown verminderde gevaarlijke luchtverontreinigende stoffen in vijf Indiase steden tot 54 procent Hoe gaat het Amazone-regenwoud om met droogte?
Hoe gaat het Amazone-regenwoud om met droogte?  Hoe wordt een Liana -wijnstok aangepast aan het regenwoud?
Hoe wordt een Liana -wijnstok aangepast aan het regenwoud?  Onderzoekers onderzoeken hoe verschuivingen in federale benaderingen het tij van destructieve bosbranden kunnen keren
Onderzoekers onderzoeken hoe verschuivingen in federale benaderingen het tij van destructieve bosbranden kunnen keren Satellietgegevens geleide inspanning om Nepal te helpen herstellen van een reeks aardbevingen
Satellietgegevens geleide inspanning om Nepal te helpen herstellen van een reeks aardbevingen
Hoofdlijnen
- Hoe gebruiken wetenschappers de wetenschappelijke methode?
- Waar in het lichaam is het aminozuurpool?
- Hoe wordt papierboom genetisch gemodificeerd?
- Hoe reproduceert een pioen?
- De snelheid van verval berekenen
- Het sorteren en recombineren van genen tijdens meststillatie van meiosis leidt meestal tot de productie van?
- Wat is het eerste proces in cel dat wordt beïnvloed door anaërobe omstandigheden?
- Welk proces voeren Ribosomes uit?
- Hoe kan DNA -hybridisatie een maat voor genetische verwantschap tussen soorten geven?
- Smartphone-sensoren kunnen cannabishigh detecteren en hebben de potentie om vroegtijdig in te grijpen

- Dynamiek van zijde-eiwitten is de sleutel tot uitstekende stabiliteit van spinzijde als biomateriaal
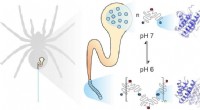
- Methaan kansrijke route voor opslag duurzame energie uit zon en wind
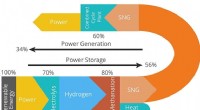
- Wetenschapper bouwt kunstmatige fotosynthetische cellen
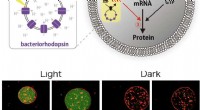
- Verbeterde reactie van het menselijk lichaam op implantaten
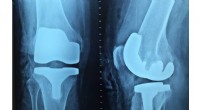
 Ontwikkeling bedreigt tropische bossen, onderzoekers zeggen:
Ontwikkeling bedreigt tropische bossen, onderzoekers zeggen: Nieuwe modellering zal licht werpen op het effect van beleidsbeslissingen op migratie door zeespiegelstijging
Nieuwe modellering zal licht werpen op het effect van beleidsbeslissingen op migratie door zeespiegelstijging Wat is de energie van een foton dat lichtfrequentie uitzendt 7.211014 Hz?
Wat is de energie van een foton dat lichtfrequentie uitzendt 7.211014 Hz?  Wat leerden wetenschappers van maanmonsters teruggebracht door Apollo Astronaunts?
Wat leerden wetenschappers van maanmonsters teruggebracht door Apollo Astronaunts?  Is een organisme geclassificeerd als persoon?
Is een organisme geclassificeerd als persoon?  Giant organisch molecuul gemaakt van kleine moleculen die aan elkaar zijn gekoppeld?
Giant organisch molecuul gemaakt van kleine moleculen die aan elkaar zijn gekoppeld?  Legitimatiestrategieën voor kolenuitgangen in Duitsland en Canada
Legitimatiestrategieën voor kolenuitgangen in Duitsland en Canada Het simuleren van vroege oceaanopeningen laat zien dat levensbouwstenen onder druk worden gevormd
Het simuleren van vroege oceaanopeningen laat zien dat levensbouwstenen onder druk worden gevormd
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

