
Wetenschap
Wat is de naam van hybride orbitalen die door zwavel in SCL2 worden gebruikt?
De hybride orbitalen die door zwavel in SCL₂ worden gebruikt, zijn sp³
Dit is waarom:
* Sulphur's Electron Configuration: Zwavel heeft 6 valentie -elektronen (3s² 3p⁴).
* binding in SCL₂: Zwavel vormt twee enkele bindingen met twee chlooratomen.
* Hybridisatie: Om de twee bindingsparen en twee eenzame paren elektronen rond zwavel te huisvesten, ondergaat het SP³ hybridisatie. Dit creëert vier equivalente SP³ hybride orbitalen, waarbij twee de enige paren vasthouden en de andere twee overlappende met de chloororbitalen om de S-CL-bindingen te vormen.
 Waarom je geen vrijhandel kunt hebben en de planeet kunt redden?
Waarom je geen vrijhandel kunt hebben en de planeet kunt redden? Onderzoekers constateren dat bommen uit de Eerste en Tweede Wereldoorlog in de grond vluchtiger worden
Onderzoekers constateren dat bommen uit de Eerste en Tweede Wereldoorlog in de grond vluchtiger worden  Uit onderzoek blijkt hoe gewasprijzen en klimaatvariabelen het opbrengstareaal beïnvloeden
Uit onderzoek blijkt hoe gewasprijzen en klimaatvariabelen het opbrengstareaal beïnvloeden  Typen Ouderwetse Weerinstrumenten
Typen Ouderwetse Weerinstrumenten Hoe de waterradfabriek knapt
Hoe de waterradfabriek knapt
Hoofdlijnen
- Welke rol speelt de eerste wet van de thermodynamica in levende organismen?
- Wat worden bekers gebruikt om te meten?
- Wat is cyberchondrie?
- Vier nieuwe caladiumcultivars voor containers en landschappen
- Vergeet mammoeten, onderzoek laat zien hoe je ratten op Christmas Island weer tot leven kunt wekken
- Welke invloed heeft de zuurschok in het voorjaar op waterorganismen?
- Onderzoek laat zien hoe planten de ‘herinnering’ aan een hoog kooldioxidegehalte doorgeven aan hun nakomelingen
- Wat bevat eiwitten?
- Wat beweegt langs het mRNA en helpt peptide -streng te vormen?
- Beheersing van vitamine K2-productie in de tuberculosebacterie

- Kleine elektrische velden kunnen een beslissende rol spelen bij de vorming van diamant

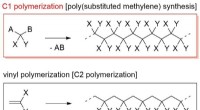
- Ontwikkeling van nieuwe slimme zachte materialen:Synthese van een pH-responsief gedendroniseerd poly(gesubstitueerd methyleen)s
- Nieuwe chemie maakt verbeteringen aan magische medicijnen gemakkelijker

- Waterdruppels als geminiaturiseerde reageerbuisjes

 Hebben de Apollo -missies mensen op Mercurius geland?
Hebben de Apollo -missies mensen op Mercurius geland?  Wat is niet-fundamentele kracht?
Wat is niet-fundamentele kracht?  Is ooggrootte gerelateerd aan genetica of omgeving?
Is ooggrootte gerelateerd aan genetica of omgeving?  Wat is de omvang van zwaartekrachten vierce tussen twee 1 kilogramlichamen die uit elkaar zijn?
Wat is de omvang van zwaartekrachten vierce tussen twee 1 kilogramlichamen die uit elkaar zijn?  Wat doet een geoloog?
Wat doet een geoloog?  In welke soorten rotsen zijn olieafzettingen meestal aangetroffen?
In welke soorten rotsen zijn olieafzettingen meestal aangetroffen?  Wat is de betekenis van voorspellen in de wetenschap?
Wat is de betekenis van voorspellen in de wetenschap?  Wat is een onuitputtelijke energiebron?
Wat is een onuitputtelijke energiebron?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

