
Wetenschap
De polariteit van ammoniak begrijpen:vorm en elektronegativiteit
1. Asymmetrische vorm: Het ammoniakmolecuul heeft een trigonale piramidevorm , waarbij het stikstofatoom aan de top staat en de drie waterstofatomen de basis vormen. Deze vorm is te wijten aan het eenzame elektronenpaar op het stikstofatoom, dat de bindingsparen afstoot, waardoor het molecuul afwijkt van een perfect tetraëdrische opstelling.
2. Verschil in elektronegativiteit: Stikstof is elektronegatiever dan waterstof. Dit betekent dat stikstof een sterkere aantrekkingskracht uitoefent op de gedeelde elektronen in de NH-bindingen, waardoor een gedeeltelijke negatieve lading (δ-) op het stikstofatoom en gedeeltelijke positieve ladingen (δ+) op de waterstofatomen ontstaat.
3. Netto dipoolmoment: Vanwege de asymmetrische vorm en het verschil in elektronegativiteit heffen de individuele bindingsdipolen in de N-H-bindingen elkaar niet op. In plaats daarvan worden ze bij elkaar opgeteld om een netto dipoolmoment te creëren wijzend naar het stikstofatoom. Dit netto dipoolmoment maakt het ammoniakmolecuul polair.
Samengevat: De combinatie van de asymmetrische vorm, het elektronegativiteitsverschil en het resulterende netto dipoolmoment maakt het ammoniakmolecuul polair. Deze polariteit is cruciaal voor veel eigenschappen van ammoniak, waaronder het vermogen om waterstofbruggen te vormen en de hoge oplosbaarheid in water.
 Welke van deze eigenschappen kan een onbekende vloeistof worden gevonden met behulp van een bekerverwarmingsplaat en temperatuursonde?
Welke van deze eigenschappen kan een onbekende vloeistof worden gevonden met behulp van een bekerverwarmingsplaat en temperatuursonde?  Hoe lichtdeeltjes druppels de perfecte vloeistof kunnen produceren
Hoe lichtdeeltjes druppels de perfecte vloeistof kunnen produceren  Wat is het totale aantal atomen in chromaat?
Wat is het totale aantal atomen in chromaat?  Waterstofverbranding:oxidatie, bindingsvorming en waterproductie
Waterstofverbranding:oxidatie, bindingsvorming en waterproductie  Welke koolstof is uniek vanwege de atomen?
Welke koolstof is uniek vanwege de atomen?
 Langer modderseizoen, geen sneeuw zou de noordoostelijke rivieren kunnen veranderen tegen het jaar 2100
Langer modderseizoen, geen sneeuw zou de noordoostelijke rivieren kunnen veranderen tegen het jaar 2100 Gevaarlijke hittegolven zullen de tropen waarschijnlijk dagelijks teisteren tegen 2100:studie
Gevaarlijke hittegolven zullen de tropen waarschijnlijk dagelijks teisteren tegen 2100:studie Vulkaan bij Tokio barst uit, waarschuwingen oproepen
Vulkaan bij Tokio barst uit, waarschuwingen oproepen Groter is soms beter als het gaat om de grootte van de boerderij
Groter is soms beter als het gaat om de grootte van de boerderij Wat zijn zes voorbeelden van eigenschappen?
Wat zijn zes voorbeelden van eigenschappen?
Hoofdlijnen
- Waarom zijn vis belangrijk voor het ecosysteem?
- Een celbioloog behandelt een zodat zuurstof niet kan diffunderen over het membraan welke organel hierdoor rechtstreeks zal worden beïnvloed?
- Hoe bacteriën spuiten maken:wetenschappers reconstrueren het bacteriële transportkanaal in reageerbuisjes
- Wat voor soort symbiose is waar beide organismen profiteren?
- Hoe mRNA de kern verlaat:de weg naar eiwitproductie
- Prokaryotische cellen identificeren:belangrijkste kenmerken en afwezigheid van een kern
- Wat beschrijft een worm die de lichamen van dode organisme afbreekt?
- Waarom is vertaling afhankelijk van transcriptie?
- Welke rol heeft de kern in een dierencel?
- Een nieuwe manier om MXene-films te maken die elektromagnetische interferentie blokkeren

- Onderzoek naar roamingreacties om nieuw licht te werpen op atmosferische moleculen

- Verdamping versus koken:de twee belangrijkste vormen van verdamping

- Biovriendelijke protocellen pompen bloedvaten op

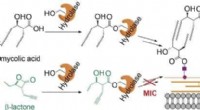
- Antibacteriële bèta-lacton infiltreert in de biosynthese van het mycomembraan en doodt de ziekteverwekker van tuberculose
 Soorten ophaalbruggen
Soorten ophaalbruggen Hoe verschilt een cel van andere cellen?
Hoe verschilt een cel van andere cellen?  5 Basisbehoeften van een dier
5 Basisbehoeften van een dier  Vermogen van een object om te trillen door energie te absorberen bij zijn natuurlijke frequentie?
Vermogen van een object om te trillen door energie te absorberen bij zijn natuurlijke frequentie?  Een stof met een vast volume en vorm?
Een stof met een vast volume en vorm?  Wanneer licht wordt geabsorbeerd energie omgezet in winkelsergie?
Wanneer licht wordt geabsorbeerd energie omgezet in winkelsergie?  Wat is het levensverhaal van een ster?
Wat is het levensverhaal van een ster?  Klein stuk van een ziekteverwekker dat een immuunrespons genereert?
Klein stuk van een ziekteverwekker dat een immuunrespons genereert?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

