
Wetenschap
Waterstofverbranding:oxidatie, bindingsvorming en waterproductie
De reactie:
2 H₂ (g) + O₂ (g) → 2 H₂O (l)
Oxidatie:
* Waterstof (H₂) wordt geoxideerd. Oxidatie is het verlies van elektronen. Bij deze reactie verliest elk waterstofatoom een elektron en wordt een waterstofion (H⁺).
Bondvorming:
* Er worden covalente bindingen gevormd. Water (H₂O) wordt gevormd door het delen van elektronen tussen waterstof- en zuurstofatomen. Elk zuurstofatoom deelt twee elektronen met twee waterstofatomen en vormt zo twee covalente bindingen.
Uitleg:
1. Reactanten: Gasvormige waterstof (H₂) en gasvormige zuurstof (O₂) zijn de uitgangsstoffen.
2. Verbranding: Wanneer waterstof verbrandt, reageert het snel met zuurstof, waarbij energie vrijkomt in de vorm van warmte en licht.
3. Elektronenoverdracht: Waterstofatomen, die een lagere elektronegativiteit hebben dan zuurstof, verliezen elektronen en worden positief geladen (H⁺). Zuurstofatomen nemen deze elektronen op en worden negatief geladen (O²⁻).
4. Watervorming: De positief geladen waterstofionen (H⁺) en negatief geladen zuurstofionen (O²⁻) trekken elkaar aan en vormen covalente bindingen, waardoor watermoleculen (H₂O) ontstaan.
Samenvatting:
* Geoxideerd molecuul: Waterstof (H₂)
* Bond gevormd: Covalente bindingen in het watermolecuul (H₂O)
 Wat gebeurt er als de kaliumpermanganaatoplossing daalt naar water?
Wat gebeurt er als de kaliumpermanganaatoplossing daalt naar water?  Wat is de evenwichtige reactie wanneer lood II nitraat gemengd met calciumchloride?
Wat is de evenwichtige reactie wanneer lood II nitraat gemengd met calciumchloride?  Wat heeft de meest vergelijkbare chemische eigenschappen als broom?
Wat heeft de meest vergelijkbare chemische eigenschappen als broom?  Waar is alumiuim van gemaakt?
Waar is alumiuim van gemaakt?  Welk zuur is een sterke elektrolyt A. zwavelzuur B. azijnzuur C. mierenzuur D. citroenzuur?
Welk zuur is een sterke elektrolyt A. zwavelzuur B. azijnzuur C. mierenzuur D. citroenzuur?
 Continenten die in hun kindertijd vatbaar zijn voor vernietiging, studie vondsten
Continenten die in hun kindertijd vatbaar zijn voor vernietiging, studie vondsten Duitsland zet 100 miljard euro in voor klimaat terwijl protesten oplaaien
Duitsland zet 100 miljard euro in voor klimaat terwijl protesten oplaaien Zijn natuurlijke vezels echt beter voor het milieu dan microplastic vezels?
Zijn natuurlijke vezels echt beter voor het milieu dan microplastic vezels? Hoe is de studie van een klein blad dat wordt genoemd?
Hoe is de studie van een klein blad dat wordt genoemd?  Paus spoort Republikeinen aan om klimaatvisie te veranderen
Paus spoort Republikeinen aan om klimaatvisie te veranderen
Hoofdlijnen
- Wat is de functie van Branchi?
- Wat zijn de drie klieren van een reproductief systeem voor mannen?
- Eukaryoten versus prokaryoten:belangrijkste verschillen verklaard
- Wat is de gespecialiseerde plantencel die water draagt?
- Wat is de rol van microfilamenten bij celdeling?
- Welk type menselijke cellen bevatten geen kernen?
- Kolonies in verval:wat veroorzaakt de massale sterfte van honingbijen?
- Wat gebeurt er als nieuwe gegevens de huidige wetenschappelijke verklaringen in Qeustion noemen?
- Organisme wiens cellen altijd of meestal een kern bevatten, worden wat genoemd?
- Ingenieurs gebruiken warmtevrije technologie om metalen replica's te maken van een oppervlaktetextuur van rozen

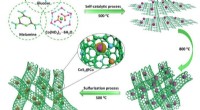
- S, N co-gedoteerde koolstof nanobuis ingekapselde CoS2@Co
- Hoe u de titreerbare zuurgraad in wijn kunt berekenen:een stapsgewijze handleiding

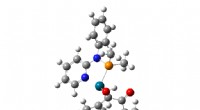
- Supercomputing van het hoe van chemische reacties
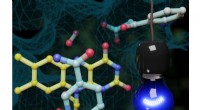
- Onderzoekers triggeren enzymen met licht
 Welke twee dingen moeten mechanische golven altijd door reizen?
Welke twee dingen moeten mechanische golven altijd door reizen?  Antarctische ijskappen lopen een groter risico om te smelten dan eerder werd gedacht
Antarctische ijskappen lopen een groter risico om te smelten dan eerder werd gedacht Wat is de relatie tussen snelheid en gebied?
Wat is de relatie tussen snelheid en gebied?  Zwavel wordt voornamelijk gedolven voor de productie van?
Zwavel wordt voornamelijk gedolven voor de productie van?  Case 1070 Tractorspecificaties
Case 1070 Tractorspecificaties Bewustzijn is barrière voor plasticvrije periodes
Bewustzijn is barrière voor plasticvrije periodes Wat gebeurt er als een spoel tussen twee magneten wordt gedraaid?
Wat gebeurt er als een spoel tussen twee magneten wordt gedraaid?  Als je een bal in de lucht gooit op winderige dagbeweging van je arm is kracht die invloed heeft op de vliegpad Welke andere krachten bal?
Als je een bal in de lucht gooit op winderige dagbeweging van je arm is kracht die invloed heeft op de vliegpad Welke andere krachten bal?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

