
Wetenschap
Kopercorrosie en pH:een hypothese over de zuurgraad van water
Hypothese:
De snelheid van kopercorrosie zal toenemen naarmate de pH van het water afneemt (zuurder wordt).
Uitleg:
Kopercorrosie wordt voornamelijk veroorzaakt door elektrochemische reacties waarbij koperatomen elektronen verliezen en geoxideerd raken. Dit proces wordt beïnvloed door de aanwezigheid van opgeloste zuurstof en waterstofionen (H+) in het water.
* Zure omgevingen (lage pH): Hogere concentraties H+-ionen in zuur water versterken de elektrochemische reacties door een grotere drijvende kracht te bieden voor koperoxidatie. Dit leidt tot een snellere corrosie.
* Alkalische omgevingen (hoge pH): In alkalische omstandigheden kan de aanwezigheid van hydroxide-ionen (OH-) een beschermende oxidelaag op het koperoppervlak vormen, waardoor corrosie wordt tegengegaan.
Daarom zal een verlaging van de pH resulteren in een hogere concentratie H+-ionen, waardoor de elektrochemische reacties worden versneld en tot verhoogde kopercorrosie leidt.
Opmerking: Dit is een algemene hypothese en de feitelijke relatie tussen pH en kopercorrosie kan complex zijn en worden beïnvloed door andere factoren zoals temperatuur, opgeloste zouten en de aanwezigheid van andere metalen.
Hoofdlijnen
- Wat zijn de twee delen van de wetenschap?
- Hoe het luisteren naar het juiste gezoem ervoor zorgt dat muggen niet met de verkeerde soort paren
- Wat is de naam van enzym die mRNA creëert?
- Wat zijn geen componenten van een nucleotide?
- Wetenschappers tonen respect voor sommige parasieten
- Komt neutralisatie in planten op de wortels?
- Wat is de strijd van organismen voor dezelfde beperkte middelen die worden genoemd?
- Wat is een virus dat onmiddellijk invloed heeft op gastheercelfuncties?
- Dominante organismen in tertiaire periode?
- Chemici hebben verbindingen gemaakt die glaucoom kunnen behandelen
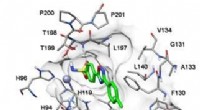
- Onderzoekers ontwikkelen katalysator die het Z-schema van fotosynthese nabootst

- Nieuwe biofarmaceutische kwaliteitscontrolemethode bij testen
- Onderzoekers melden een nieuw en beter soort onzichtbare inkt

- Superstaalproject bereikt grote doorbraak

 De hitte is aan:wat we weten over waarom de oceaantemperaturen records blijven breken
De hitte is aan:wat we weten over waarom de oceaantemperaturen records blijven breken  Wat is het woordvergelijking voor cesiumchloride?
Wat is het woordvergelijking voor cesiumchloride?  Is draad een isolator of geleider?
Is draad een isolator of geleider?  Wanneer een menselijk embryo wordt gevormd welk systeem het eerst heeft gemaakt?
Wanneer een menselijk embryo wordt gevormd welk systeem het eerst heeft gemaakt?  Laat de meisjes fluit spelen, jongens bash drums stereotypen
Laat de meisjes fluit spelen, jongens bash drums stereotypen Een fosfolipidemolecuul heeft een polair en een niet-polair uiteinde. Wat voor soort binding vormen watermoleculen?
Een fosfolipidemolecuul heeft een polair en een niet-polair uiteinde. Wat voor soort binding vormen watermoleculen?  Waarom kunnen organismen in verschillende groepen van elkaar ver van elkaar zijn en toch gedeelde faturen hebben?
Waarom kunnen organismen in verschillende groepen van elkaar ver van elkaar zijn en toch gedeelde faturen hebben?  Nanokabels verlichten de weg naar de toekomst:onderzoekers voeden lijnspanningslamp met nanobuisdraad
Nanokabels verlichten de weg naar de toekomst:onderzoekers voeden lijnspanningslamp met nanobuisdraad
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


