
Wetenschap
Elektronendomein van NO2:een stapsgewijze handleiding
1. Teken de Lewis-structuur
* Stikstof (N) is het centrale atoom en heeft 5 valentie-elektronen.
* Zuurstof (O) heeft elk 6 valentie-elektronen.
De Lewis-structuur ziet er als volgt uit:
O
||
N - O
2. Tel de elektronendomeinen
Een elektronendomein is een gebied in de ruimte rond een atoom waar elektronen geconcentreerd zijn. Het kan een enkele binding, een dubbele binding, een drievoudige binding of een eenzaam elektronenpaar zijn.
* In NO2 zijn er drie elektronendomeinen rond het centrale stikstofatoom:
* Eén dubbele binding aan het linker zuurstofatoom.
* Eén dubbele binding aan het juiste zuurstofatoom.
* Eén eenzaam elektronenpaar op het stikstofatoom.
3. Bepaal de elektronendomeingeometrie
Gebaseerd op de drie elektronendomeinen is de geometrie van het elektronendomein trigonaal vlak . Dit betekent dat de elektronendomeinen in een driehoekige vorm rondom het stikstofatoom zijn gerangschikt.
Belangrijke opmerking: Terwijl de geometrie van het elektronendomein trigonaal vlak is, is de *moleculaire* geometrie van NO2 gebogen vanwege de aanwezigheid van het eenzame paar op het stikstofatoom. Eenzame paren oefenen een grotere afstotende kracht uit op de bindingsparen, waardoor het molecuul buigt.
 Genieten van het uitzicht? Hoe computerspellen kunnen helpen bij het evalueren van landschappen
Genieten van het uitzicht? Hoe computerspellen kunnen helpen bij het evalueren van landschappen Zuid-Afrika:Stijgende temperaturen zullen tot 20% van het BBP per hoofd van de bevolking kosten
Zuid-Afrika:Stijgende temperaturen zullen tot 20% van het BBP per hoofd van de bevolking kosten Europees Parlement stopt met plastic waterflessen
Europees Parlement stopt met plastic waterflessen Hoe noemde Darwin verschillende levende wezens?
Hoe noemde Darwin verschillende levende wezens?  Wat voor soort dieren leven op bladeren?
Wat voor soort dieren leven op bladeren?
Hoofdlijnen
- Kan een klein deeltje de plaag van het vergroenen van citrusvruchten tegengaan?
- Welk type wetenschap omvat de onderzoekscentrales?
- Wat zijn chemische boodschappers in de cel die de hoeveelheden geproduceerde enzym regelen?
- Hoe cellen fouten corrigeren onder tijdsdruk
- Kunnen we leren om van slakken en slakken te houden in onze tuinen?
- Seks:waarom moeite doen? Wetenschappers onderzoeken evolutionaire mysteries
- Wanneer een eindproduct van een reactieroute overmaat is en het eerste enzym remt, negatieve feedback?
- Wat is het kader waar het wetenschappelijk onderzoek door wordt bestuurd?
- Gerst is de smaak van de maand, aangezien nieuwe studie het eeuwenoude brouwdebat beslecht
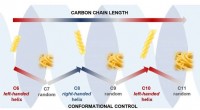
- Koolstofketens nemen fusilli- of spaghetti-vormen aan als ze oneven of even getallen hebben
- Het aantal atomen in elk monster berekenen:een duidelijke, stapsgewijze handleiding
- Onderzoekers maken kunstmatig parelmoer met behulp van bacteriën

- Superflexibele aerogels zijn zeer efficiënte absorptiemiddelen, thermische isolatoren, en druksensoren

- Big data en synthetische chemie kunnen klimaatverandering en vervuiling tegengaan

 Wat gebeurt er met de snelheid van een golf wanneer deze refracts en verschillen weerspiegelt?
Wat gebeurt er met de snelheid van een golf wanneer deze refracts en verschillen weerspiegelt?  Reisen radiogolven door vacuümfasetr dan zichtbare lichtgolven?
Reisen radiogolven door vacuümfasetr dan zichtbare lichtgolven?  Vang me als je kunt:hoe mRNA-therapieën in cellen worden afgeleverd
Vang me als je kunt:hoe mRNA-therapieën in cellen worden afgeleverd  Vorming van honingraat nanostructuren eindelijk uitgelegd
Vorming van honingraat nanostructuren eindelijk uitgelegd Kan de ene vorm van energie naar de andere worden omgezet?
Kan de ene vorm van energie naar de andere worden omgezet?  Verhogen van de effectiviteit van condensatie door electrowetting
Verhogen van de effectiviteit van condensatie door electrowetting Wat is de ideale gaswet?
Wat is de ideale gaswet?  Afbeelding:de zon laat een sterke zonnevlam los
Afbeelding:de zon laat een sterke zonnevlam los
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

