
Wetenschap
Oplossen versus reageren in water:een duidelijk onderscheid
Oplossen
* Er worden geen nieuwe stoffen gevormd. De vaste stof valt eenvoudigweg uiteen in zijn individuele ionen of moleculen, die vervolgens worden omgeven door watermoleculen.
* Het proces is meestal omkeerbaar. Vaak kunt u de oorspronkelijke vaste stof terugwinnen door het water te verdampen.
* Er wordt geen gas geproduceerd.
* Geen verandering in temperatuur (of een zeer kleine, onbeduidende verandering).
Reageren
* Er worden nieuwe stoffen gevormd. De oorspronkelijke vaste stof combineert chemisch met watermoleculen, waardoor nieuwe verbindingen ontstaan.
* Het proces is meestal niet gemakkelijk omkeerbaar. Je kunt de oorspronkelijke vaste stof niet terugkrijgen door simpelweg het water te verdampen.
* Er kan gas worden geproduceerd.
* Er is een merkbare temperatuurverandering. De oplossing kan heter worden (exotherme reactie) of kouder (endotherme reactie).
Voorbeelden:
* Oplossen: Zout (NaCl) dat oplost in water. Het zout valt uiteen in Na+ en Cl-ionen, maar de chemische samenstelling van het zout zelf is niet veranderd. Door het water te verdampen, kun je het zout terugkrijgen.
* Reageren: Natriummetaal (Na) reageert met water. Hierbij ontstaan natriumhydroxide (NaOH) en waterstofgas (H2). Het natrium heeft chemisch gereageerd met water om nieuwe stoffen te vormen. Je kunt het natrium niet simpelweg terugkrijgen door het water te verdampen.
Praktische observaties:
* Uiterlijk: Verdwijnt de vaste stof volledig in het water, of zie je zichtbare veranderingen in de oplossing (kleurverandering, troebelheid)?
* Verwarming/koeling: Voelt de oplossing warmer of kouder aan nadat de vaste stof is opgelost?
* Gasproductie: Zie jij belletjes ontstaan?
* Geur: Heeft de oplossing een nieuwe, duidelijke geur nadat de vaste stof is opgelost?
Belangrijke opmerking: Soms kan het lastig zijn om het verschil te zien tussen oplossen en reageren. Als u het niet zeker weet, kunt u altijd het beste een betrouwbare bron van chemische informatie raadplegen.
 Zuivere brandstof uit zonlicht halen
Zuivere brandstof uit zonlicht halen Hoe is Michael Faraday vloeibaar chloor?
Hoe is Michael Faraday vloeibaar chloor?  Wat is de molariteit van een 0,142 M NA3 PO4 -oplossing met een dichtheid 1.015 g m l tonen alle stappen?
Wat is de molariteit van een 0,142 M NA3 PO4 -oplossing met een dichtheid 1.015 g m l tonen alle stappen?  Een keramische resurfacing prothese voor heupgewrichten
Een keramische resurfacing prothese voor heupgewrichten Tussen koper aurum natrium en zilver wat is het meest kneedbare metaal?
Tussen koper aurum natrium en zilver wat is het meest kneedbare metaal?
 Kleilagen en verre pompen veroorzaken arseenverontreiniging in het grondwater van Bangladesh
Kleilagen en verre pompen veroorzaken arseenverontreiniging in het grondwater van Bangladesh Hoe kun je zien of iets wetenschap of niet-wetenschap is?
Hoe kun je zien of iets wetenschap of niet-wetenschap is?  Nieuwe dieptelimiet voor diepzeeholen
Nieuwe dieptelimiet voor diepzeeholen Waarom we een machine willen bouwen die de aantrekkelijkheid van mensen kan voorspellen
Waarom we een machine willen bouwen die de aantrekkelijkheid van mensen kan voorspellen  Nu de klimaatverandering in het Midwesten minder duidelijk zichtbaar is, willen parkbezoekers weten welke gevolgen de lokale hulpbronnen hebben
Nu de klimaatverandering in het Midwesten minder duidelijk zichtbaar is, willen parkbezoekers weten welke gevolgen de lokale hulpbronnen hebben
Hoofdlijnen
- Wat bepalen allelen?
- Hoe verschillen ouders en dochterscellen genetisch in meiose?
- Wetenschapper denken dat de eerste bacteriën op aarde waren?
- Wat zijn ribosomen?
- Welke organellen zijn zichtbaar onder een elektronenmicroscoop maar geen lichtmicroscoop?
- Wat zijn de kenmerken van levende organismen?
- Wat is het verschil tussen prokaryotische en eukaryote cellen?
- Hoe is vertaling in de biologie vergelijkbaar met taalvertaling?
- Noem de ziekte waar bloedcellen niet genoeg zuurstof dragen?
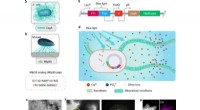
- Lichtgevoelige E. coli functionele biofilms als steigers voor hydroxyapatietmineralisatie
- Snelle identificatie van hoogwaardige, katalysatoren met meerdere elementen

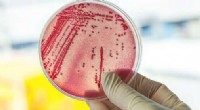
- Wetenschappers vinden nieuwe manier om te testen op resistente infecties
- Nieuwe stoffen met antivirale eigenschappen

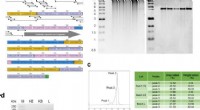
- Recombinant collageenpolypeptide als een veelzijdig biomateriaal voor bottransplantaten
 Wat gebeurt er met watermoleculen als er elektriciteit doorheen gaat tijdens elektrolyse?
Wat gebeurt er met watermoleculen als er elektriciteit doorheen gaat tijdens elektrolyse?  Hallo? Facebook lanceert telefoonapp voor Android
Hallo? Facebook lanceert telefoonapp voor Android  Met krimpende snowpack, voorspelbaarheid van droogte smelt weg
Met krimpende snowpack, voorspelbaarheid van droogte smelt weg Is het gemakkelijk om te zien dat diercellen plantencellen vormen?
Is het gemakkelijk om te zien dat diercellen plantencellen vormen?  Wie ontdekte hoe je drijvende kracht kunt bepalen?
Wie ontdekte hoe je drijvende kracht kunt bepalen?  Virgin Galactic onthult futuristische buitenpost voor ruimtetoerisme
Virgin Galactic onthult futuristische buitenpost voor ruimtetoerisme Wat is het afbreken van voedsel in energie?
Wat is het afbreken van voedsel in energie?  De opwarming van het noordpoolgebied zal de klimaatverandering versnellen en de wereldeconomie beïnvloeden
De opwarming van het noordpoolgebied zal de klimaatverandering versnellen en de wereldeconomie beïnvloeden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

