
Wetenschap
pH-indicatoren begrijpen:hoe ze werken en kleurveranderingen
Hoe indicatoren werken:
* Chemische structuur: Indicatoren zijn meestal zwakke zuren of basen met complexe chemische structuren. Ze hebben verschillende gekleurde vormen, afhankelijk van of ze geprotoneerd zijn (een waterstofion hebben, H+) of gedeprotoneerd (een waterstofion verloren hebben).
* pH-gevoeligheid: De kleurverandering in een indicator wordt veroorzaakt door een verschuiving in de pH (zuurgraad of alkaliteit) van de oplossing.
* Evenwicht: In zure oplossingen is het waarschijnlijk dat het indicatormolecuul wordt geprotoneerd, waardoor het één kleur krijgt. In basische oplossingen wordt het molecuul waarschijnlijk gedeprotoneerd, waardoor het een andere kleur krijgt.
Voorbeelden van indicatoren:
* Lakmoespapier: Wordt rood in zure oplossingen en blauw in basische oplossingen.
* Fenolftaleïne: Kleurloos in zure oplossingen en roze in basische oplossingen.
* Methyloranje: Rood in zure oplossingen en geel in basische oplossingen.
* Broomthymolblauw: Geel in zure oplossingen, groen in neutrale oplossingen en blauw in basische oplossingen.
Voorbij indicatoren:
Hoewel indicatoren het meest voorkomen, kunnen ook andere stoffen in zuren of basen van kleur veranderen, zoals:
* Sommige natuurlijke kleurstoffen: Denk aan rodekoolsap, dat rood kleurt in zuur en blauw in basis.
* Bepaalde metaalionen: Oplossingen die enkele metaalionen bevatten, kunnen van kleur veranderen afhankelijk van de pH.
Laat het me weten als je meer informatie wilt over een specifieke indicator of de chemie achter hun kleurveranderingen!
 Californië zal de CO2-reductiedoelstellingen niet halen, vernietigende audit van staatsvoorspellingen
Californië zal de CO2-reductiedoelstellingen niet halen, vernietigende audit van staatsvoorspellingen Mondiaal oppervlak van rivieren en beken is 45 procent groter dan eerder werd gedacht
Mondiaal oppervlak van rivieren en beken is 45 procent groter dan eerder werd gedacht NASA volgt extra-tropische storm Sebastien naar het VK
NASA volgt extra-tropische storm Sebastien naar het VK Hoe wordt het genoemd om menselijke kwaliteiten een object of ding te geven?
Hoe wordt het genoemd om menselijke kwaliteiten een object of ding te geven?  Kenmerken van een pauwvogel
Kenmerken van een pauwvogel
Hoofdlijnen
- Welke eiwitten werken als selectieve doorgangen in het celmembraan?
- Californische vogels nestelen een week eerder dan een eeuw geleden
- Fruitvliegonderzoek kan onthullen wat er in de hersenen van vrouwen gebeurt tijdens verkering en paring
- Wat is een voorbeeld van een ander vorm dat Gene heeft voor eigenschap?
- Welk bioom wordt ook mediterraan genoemd?
- Noem die groep organismen die niet netjes past in een schema -classificatie?
- Hoe kan de evolutie van een kenmerk binnen de ene soort de evelutiekarakter van een andere soort beïnvloeden?
- Welke dieren hebben witte sclera?
- Wat is een andere naam voor genen?
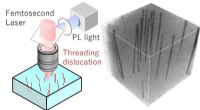
- Niet-destructieve karakteriseringstechniek helpt bij de ontwikkeling van galliumnitridekristallen
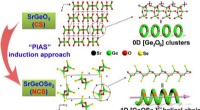
- Nieuwe gedeeltelijke isovalente inductiestrategie voor anionsubstitutie om infrarood niet-lineaire optische materialen te ontwerpen
- Onderzoekers ontwikkelen flexibel kristal, de weg vrijmaken voor efficiëntere buigbare elektronica

- Nieuw membraanwaterbehandelingssysteem om giftig afval en afvalverwerkingskosten met meer dan 90 procent te verminderen

- Onderzoek naar een thermische uitdaging voor MOF's

 stadstuinen, openbare producten staan gemakkelijk voedsel woestijn ellende
stadstuinen, openbare producten staan gemakkelijk voedsel woestijn ellende Wie is een 19e -eeuwse astronoom die zijn naam aan temperatuurschaal gaf?
Wie is een 19e -eeuwse astronoom die zijn naam aan temperatuurschaal gaf?  Wat zijn twee of meer krachten als er effecten elkaar annuleren en ze geen verandering veroorzaken in een objectenbeweging?
Wat zijn twee of meer krachten als er effecten elkaar annuleren en ze geen verandering veroorzaken in een objectenbeweging?  Acetaten? - Antwoorden
Acetaten? - Antwoorden  Wat als we de oorlog zouden beëindigen?
Wat als we de oorlog zouden beëindigen?  Waarom lijkt de zon 's nachts te verdwijnen?
Waarom lijkt de zon 's nachts te verdwijnen?  Studie onderzoekt hoe herbicide bijdraagt aan het fosforgehalte in bodem en waterwegen
Studie onderzoekt hoe herbicide bijdraagt aan het fosforgehalte in bodem en waterwegen Wat is de definitie van mealing in wetenschappelijke vorm?
Wat is de definitie van mealing in wetenschappelijke vorm?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

