
Wetenschap
Inzicht in de liquefactie van ammoniak:intermoleculaire krachten en omstandigheden
* Sterke intermoleculaire krachten: Ammoniakmoleculen (NH3) zijn polair, wat betekent dat ze een positief en een negatief uiteinde hebben vanwege het elektronegativiteitsverschil tussen stikstof en waterstof. Deze polariteit zorgt voor sterke dipool-dipoolinteracties tussen moleculen. Bovendien kan ammoniak waterstofbruggen vormen, wat nog sterkere intermoleculaire krachten zijn.
* Druk en temperatuur:
* Druk: Door de druk te verhogen, worden de moleculen dichter bij elkaar gebracht, waardoor de sterkte van de intermoleculaire krachten toeneemt.
* Temperatuur: Het verlagen van de temperatuur vermindert de kinetische energie van de moleculen, waardoor het voor de intermoleculaire krachten gemakkelijker wordt om de beweging van de moleculen te overwinnen en ze in vloeibare toestand bij elkaar te houden.
Liquefactieproces:
Wanneer ammoniakgas wordt blootgesteld aan zowel verhoogde druk als verlaagde temperatuur, gebeurt het volgende:
1. De moleculen vertragen door de lagere temperatuur.
2. De verhoogde druk dwingt de moleculen dichter bij elkaar.
3. De sterke intermoleculaire krachten worden dominant en overwinnen de kinetische energie van de moleculen.
4. De gasmoleculen gaan over in een meer gecondenseerde, vloeibare toestand.
Samenvattend wordt ammoniakgas vloeibaar door de combinatie van sterke intermoleculaire krachten (dipool-dipool- en waterstofbinding) en gunstige druk- en temperatuuromstandigheden.
 Welke factoren moeten gelijk zijn bij een omkeerbare chemische reactie bij evenwicht?
Welke factoren moeten gelijk zijn bij een omkeerbare chemische reactie bij evenwicht?  Magnesiumchloride (MgCl2):eigenschappen en kristalstructuur
Magnesiumchloride (MgCl2):eigenschappen en kristalstructuur  Smelt plastic flessen voor Molding
Smelt plastic flessen voor Molding Wat gebeurt er in elke indivdual haarschacht wanneer een anilinedivatieve tint wordt gemengd met waterstofperoxide?
Wat gebeurt er in elke indivdual haarschacht wanneer een anilinedivatieve tint wordt gemengd met waterstofperoxide?  Welke heeft een hoger smeltpunt natriumchloride of ethylalcohol?
Welke heeft een hoger smeltpunt natriumchloride of ethylalcohol?
 Welke soorten fronten vormen een onweersbui?
Welke soorten fronten vormen een onweersbui?  Schotland zegt nee tegen fracken
Schotland zegt nee tegen fracken Gegevensassimilatie verbetert de voorspellingen van aerosolen en gasvormige verontreinigende stoffen in heel China aanzienlijk
Gegevensassimilatie verbetert de voorspellingen van aerosolen en gasvormige verontreinigende stoffen in heel China aanzienlijk Testen hoe zeewierbiofilters de waterkwaliteit van het Great Barrier Reef kunnen verbeteren
Testen hoe zeewierbiofilters de waterkwaliteit van het Great Barrier Reef kunnen verbeteren  De langetermijneffecten van COVID-19 op klimaatverandering - ten goede of ten kwade
De langetermijneffecten van COVID-19 op klimaatverandering - ten goede of ten kwade
Hoofdlijnen
- Effectieve technieken voor het kweken van bacteriën op agar
- Wat kan er gebeuren met menselijke bloedcellen als ze in een beker van zout water worden geplaatst?
- Welke twee gepaarde celstructuren worden gekopieerd voordat de mitose begint?
- Hoe heet het proces waarbij delingscellen haploïde cellen vormen?
- Welk type ziekte dat organisme veroorzaakt, is zo klein dat je een microscoop moet gebruiken om het te zien?
- Wat is de functie van Petiole?
- Wat is biofysisch onderzoek?
- Wanneer een regenworm zich van het licht keert, welk kenmerk van levende dingen is dat?
- Wat zijn de verschillende niveaus van organisaties in een organisme?
- Molariteit beheersen:een stapsgewijze handleiding voor het berekenen van mol per liter

- Nieuw concept voor het identificeren van chemische combinaties met mogelijke gezondheidseffecten

- De onderbuik van kreeften is net zo sterk als industrieel rubber

- Chemici zien een vluchtige overgangstoestand van een reactie

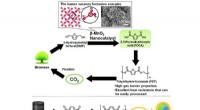
- Groene katalysatoren met aardrijke metalen versnellen de productie van biobased plastic
 Wat is instandhouding ploegen?
Wat is instandhouding ploegen?  Een wetenschapper heeft een hypothese dat de maan afbrak van een andere planeet die door de ruimte dreef en verstrikt raakte in zwaartekrachttrekkingen, heeft dit potentieel om de te worden?
Een wetenschapper heeft een hypothese dat de maan afbrak van een andere planeet die door de ruimte dreef en verstrikt raakte in zwaartekrachttrekkingen, heeft dit potentieel om de te worden?  Wat is de puurste vorm van kwik?
Wat is de puurste vorm van kwik?  Snel roterende sterren in het centrum van de Melkweg zouden vanuit de buitenwijken van de melkweg zijn gemigreerd
Snel roterende sterren in het centrum van de Melkweg zouden vanuit de buitenwijken van de melkweg zijn gemigreerd Hoe reproduceren schimmels paddenstoelen?
Hoe reproduceren schimmels paddenstoelen?  Historisch gezien geven zwarte hogescholen afgestudeerden een loonsverhoging
Historisch gezien geven zwarte hogescholen afgestudeerden een loonsverhoging SpaceX verovert de vlag, Boeing verslaan in kosmische wedstrijd
SpaceX verovert de vlag, Boeing verslaan in kosmische wedstrijd Het antwoord op werkstress? Waarom, een huisdier!
Het antwoord op werkstress? Waarom, een huisdier!
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

