
Wetenschap
Welke heeft een hoger smeltpunt natriumchloride of ethylalcohol?
* ionische binding: Natriumchloride is een ionische verbinding. Het vormt een sterk kristalrooster dat bij elkaar wordt gehouden door elektrostatische krachten tussen positief geladen natriumionen (Na+) en negatief geladen chloride-ionen (Cl-). Deze sterke bindingen vereisen veel energie om te breken, wat resulteert in een hoog smeltpunt (801 ° C).
* waterstofbinding: Ethylalcohol is een covalente verbinding met waterstofbinding. Hoewel waterstofbinding een sterke intermoleculaire kracht is, is het aanzienlijk zwakker dan de ionische bindingen in natriumchloride. De zwakkere bindingen in ethylalcohol vereisen minder energie om te breken, waardoor het een veel lager smeltpunt heeft (-114 ° C).
Samenvattend: De sterke ionische bindingen in natriumchloride maken het een vaste stof bij kamertemperatuur en geven het een zeer hoog smeltpunt. Ethylalcohol, met zijn zwakkere waterstofbindingen, is een vloeistof bij kamertemperatuur en smelt bij een veel lagere temperatuur.
Hoofdlijnen
- Wat is een bioom en wat zijn de belangrijkste factoren die het type in een deelwereld bepalen?
- Verplaats fagocytose stoffen uit een cel?
- Die niet als micro-organismen worden beschouwd Helminten b. Schimmels c. Bacteriën d. Rickettsiae?
- Wanneer werden de capsules van bacteriën ontdekt?
- De rol van oxytocinen in relaties tussen mensen kan worden gedeeld met andere primaten
- Welke voedingsstof is essentieel voor reproductie en onderhoud van de cellulaire constructie?
- Waarom laten luipaardhaaien hun witte buik zien in Zuid-Californië? Studentonderzoekers zijn met de zaak bezig
- Hoe zijn de producten van fotosynthese gerelateerd aan celademhaling?
- Hoe de darmen aan hun villi kwamen:bij het vergelijken van soorten onderzoeken onderzoekers een proces dat zij 'vervilting' noemen
- Een nieuwe bètavoltaïsche technologie met kleurstoffen voor een betere energieproductie

- Water speelt een onverwachte rol bij de vorming van mineralen
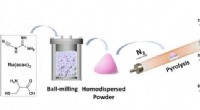
- Nieuwe katalyse met één atoom zorgt voor reductieve amineringsreactie
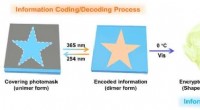
- Nieuwe fluorescerende organohydrogel voorgesteld om dubbele informatie-encryptie te bereiken
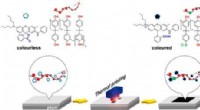
- Een stap in de richting van het kwijtraken van kassabonnen van BPA
 Wat gebeurt er als Solar Wind de aarde raakt?
Wat gebeurt er als Solar Wind de aarde raakt?  Wetenschappers persen katalysatoren in gastheermaterialen zoals een schip in een fles
Wetenschappers persen katalysatoren in gastheermaterialen zoals een schip in een fles Multifunctionele metalens ontgrendelt met licht
Multifunctionele metalens ontgrendelt met licht In welke laag van de sfeer is MT Everest?
In welke laag van de sfeer is MT Everest?  Levensduur van brandstofcellen gemaximaliseerd met kleine hoeveelheden metalen
Levensduur van brandstofcellen gemaximaliseerd met kleine hoeveelheden metalen Wat veroorzaakt de explosieve afgifte van energie in de bliksemschicht?
Wat veroorzaakt de explosieve afgifte van energie in de bliksemschicht?  Wat moet u opgeven bij het beschrijven van de snelheid van een object?
Wat moet u opgeven bij het beschrijven van de snelheid van een object?  Welke wordt veroorzaakt door Suns Energy?
Welke wordt veroorzaakt door Suns Energy?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


