
Wetenschap
Berekening van de pH van een bufferoplossing (HNO₂ en NaNO₂)
De chemie begrijpen
* HNO₂ is een zwak zuur: Het ioniseert slechts gedeeltelijk in oplossing.
* NaNO₂ is het zout van zijn geconjugeerde base: Het levert het nitrietion (NO₂⁻), dat de geconjugeerde base is van HNO₂.
* De aanwezigheid van zowel het zwakke zuur als zijn geconjugeerde base creëert een bufferoplossing: Deze oplossing is bestand tegen veranderingen in de pH.
De Henderson-Hasselbalch-vergelijking
We gebruiken de Henderson-Hasselbalch-vergelijking om de pH van deze bufferoplossing te berekenen:
pH =pKa + log([geconjugeerde base]/[zuur])
1. Bereken de pKa van HNO₂:
*De pKa van salpeterigzuur (HNO₂) is ongeveer 3,14. U kunt deze waarde vinden in een tabel met zuurdissociatieconstanten (Ka-waarden).
2. Voer de concentraties in:
* [zuur] =[HNO₂] =0,16 M
* [geconjugeerde base] =[NO₂⁻] =0,50 M
3. Bereken de pH:
pH =3,14 + log(0,50 / 0,16)
pH =3,14 + log(3,125)
pH ≈ 3,14 + 0,49
pH ≈ 3,63
Daarom is de pH van de oplossing ongeveer 3,63.
 Waarom heeft een oplossing van 0,10 molaliteit van NaCl een hoger kookpunt en lager bevriezing dan C6H12O6?
Waarom heeft een oplossing van 0,10 molaliteit van NaCl een hoger kookpunt en lager bevriezing dan C6H12O6?  Wetenschappers zetten de oplossing in een oplosmiddel voor de uitdaging van lithium-zwavelbatterijen
Wetenschappers zetten de oplossing in een oplosmiddel voor de uitdaging van lithium-zwavelbatterijen Wat is de uitgebalanceerde vergelijking voor de reactie van salpeterzuur en natriumhydroxide?
Wat is de uitgebalanceerde vergelijking voor de reactie van salpeterzuur en natriumhydroxide?  Wat doet desinfectiemiddel als chemische stof?
Wat doet desinfectiemiddel als chemische stof?  Geef een voorbeeld van hoe cohesie tussen watermoleculen belangrijk is voor levende wezens?
Geef een voorbeeld van hoe cohesie tussen watermoleculen belangrijk is voor levende wezens?
Hoofdlijnen
- Wat is een voorbeeld van parasitisme in het zoetwaterbioom?
- Hoe overleeft een plant met weinig partners of bestuivers? Een Europees kruid heeft zijn eigen weg gevonden
- Waar bevindt het amylase -enzym zich?
- Welke van de landen hebben wetenschappers onlangs muizen opgericht door twee genetische moeders en geen vaders te gebruiken?
- Wat is het tegenovergestelde van homozygote dominant?
- Waarom hebben organismen voedsel nodig?
- Is het waar dat weefsels groepen vergelijkbare cellen zijn, een specifieke functie uitvoeren in een organisme?
- Juice:Waarom duurt het zo lang?
- Wat is de basisstructuur en functie van suikers?
- Leveren van duurzaam geproduceerde bouwstenen van biomateriaal uit plantaardige grondstoffen

- Ingenieur patenteert waterachtig polymeer om keramiek op hoge temperatuur te maken
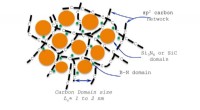
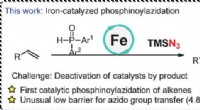
- PcFe-gekatalyseerde radicale fosfinoylazidatie van alkenen met een snelle azido-overdrachtsstap
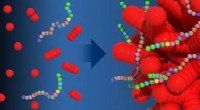
- Koraalvormige nanodeeltjes gebouwd door ontwerp met behulp van gemanipuleerde peptoïden
- Natuurlijke stoffen zijn veelbelovend tegen het coronavirus

 Wat is de chemische naam voor BRO4?
Wat is de chemische naam voor BRO4?  Van een hele dag leren tot 30 minuten per dag:de effecten van schoolsluitingen op kleuters
Van een hele dag leren tot 30 minuten per dag:de effecten van schoolsluitingen op kleuters Verdunning en hydroniumionconcentratie:een scheikundige uitleg
Verdunning en hydroniumionconcentratie:een scheikundige uitleg  Wat voor soort dieren zou je zien in een regenwoud?
Wat voor soort dieren zou je zien in een regenwoud?  Zullen cellen in het menselijk lichaam bevriezen?
Zullen cellen in het menselijk lichaam bevriezen?  Wat zijn intercellulaire bijlagen?
Wat zijn intercellulaire bijlagen?  Nieuwe klasse van veelzijdige, hoogwaardige kwantumdots klaar voor medische beeldvorming, kwantumcomputer
Nieuwe klasse van veelzijdige, hoogwaardige kwantumdots klaar voor medische beeldvorming, kwantumcomputer Wat bepaalt de grootte van kristallen die zich vormen in een monstergraniet?
Wat bepaalt de grootte van kristallen die zich vormen in een monstergraniet?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

