
Wetenschap
Wetenschappers zetten de oplossing in een oplosmiddel voor de uitdaging van lithium-zwavelbatterijen
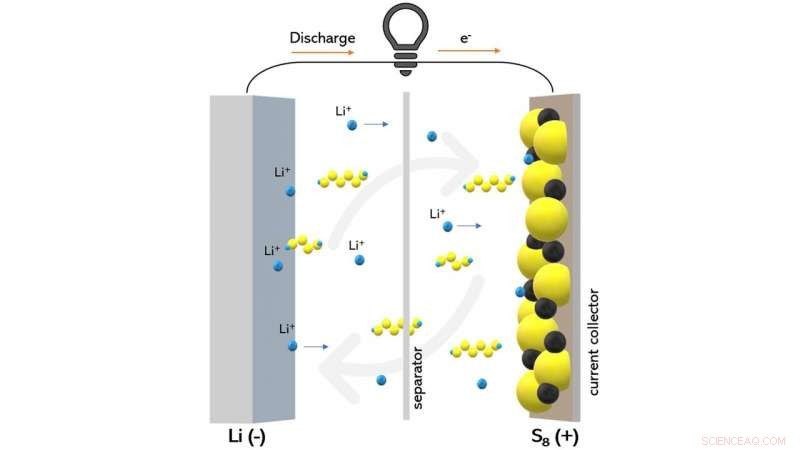
Dit diagram toont een lithium-zwavelbatterij tijdens het ontladen. Wetenschappers hebben kunnen observeren hoe een bepaald type elektrolytmateriaal het pendelen van polysulfideverbindingen (weergegeven als gele en blauwe ketens) kan verminderen, wat de prestaties van de batterij schaadt. Krediet:Wikipedia/Creative Commons
Lithium-ionbatterijen vertegenwoordigen de meerderheid van de batterijen in consumentenelektronica en elektrische voertuigen. Vandaag, wetenschappers zijn op zoek naar nieuwe chemische stoffen die de energiedichtheid en prestaties van batterijen kunnen verbeteren in vergelijking met conventionele lithium-ionbatterijen.
Een type van deze batterijen, lithium-zwavelbatterijen genoemd, zou meer energiedichtheid en lagere kosten kunnen bieden dan de traditionele grafiet/metaaloxide lithium-ionbatterij. Echter, zijn prestaties worden vaak aangetast door een parasitaire reactie die plaatsvindt in de batterij, waardoor deze niet zo efficiënt kan fietsen.
Nutsvoorzieningen, in een nieuwe studie, wetenschappers van het Argonne National Laboratory van het Amerikaanse Department of Energy hebben ontdekt hoe een bepaalde klasse elektrolytmateriaal de frequentie van deze reactie kan verminderen, mogelijk de weg vrijmaakt voor effectievere lithium-zwavelbatterijen.
Wanneer een lithium-zwavelbatterij wordt opgeladen, een onvermijdelijke nevenreactie genaamd lithium-polysulfide-shuttle komt vaak voor. Terwijl de batterij oplaadt, lithiumsulfide wordt op de kathode omgezet in zwavel, maar sommige lithium-zwavelverbindingen die onvolledig geoxideerd zijn, kunnen van de kathode oplossen in de elektrolyt - het vloeibare deel van de batterij dat de twee elektroden scheidt.
Op dit punt, de lithium-zwavelverbindingen kunnen diffunderen en gereduceerd worden op de anode en terug oxideren op de kathode. Dit proces kan keer op keer plaatsvinden op een manier die de lading van de batterij verspilt zonder deze aan het werk te zetten.
"Met de polysulfide-shuttle, je haalt niets uit je batterij, behalve om hem op te warmen, " zei de chemicus Chi Cheung Su uit Argonne, een auteur van de studie. "In elektrochemische termen, het is alsof je probeert te vliegen van New York naar Los Angeles, maar vast komen te zitten heen en weer reizen tussen Chicago en Denver."
Een groot deel van de reden voor de initiatie van het pendelen van polysulfiden vindt plaats omdat de polysulfiden gemakkelijk kunnen oplossen in een elektrolyt dat een oplosmiddelmengsel bevat van twee verbindingen genaamd dioxolaan (DOL) en dimethoxyethaan (DME). "Er zijn twee problemen die we tegelijkertijd moeten oplossen:een lage oplosbaarheid en een hoge geleidbaarheid, " zei Su. "Door beide te bereiken, we kunnen deze batterijen dichter bij de realiteit brengen."
Volgens Su, in de afgelopen vijf jaar is er een nieuw type elektrolytmateriaal ontwikkeld dat beide problemen zou kunnen aanpakken. Dit materiaal, een hydrofluorether genoemd, of HFE, heeft een veel lager oplossend vermogen terwijl het over het algemeen een goede geleidbaarheid behoudt. "De eerste stap voor het lithium om bij de anode te komen, is het oplossen in de elektrolyt, " zei hij. "Zoals water een heel goed oplosmiddel is voor tafelzout, DME is een zeer goed oplosmiddel voor lithium. Maar met HFE's is het alsof je zout in benzine probeert op te lossen."
Hoewel deze algemene eigenschap van HFE's al enkele jaren bekend is, Su en zijn collega's hebben een algemene manier bedacht om het solvatatiegedrag en de geleidbaarheid van deze klasse moleculen te voorspellen. Eerst, ze verdeelden ze in drie soorten, afhankelijk van hun chemische structuur. Bij het meten hoe de elektrolyten presteerden, de onderzoekers merkten een belangrijke wisselwerking op:die chemieën die het laagste solvaterende gedrag vertoonden en de minste hoeveelheid polysulfide-shuttling hadden ook een lagere geleidbaarheid.
"Het laat zien dat er nog geen wondermiddel is voor lithium-zwavelbatterijen, en dat we nog steeds manieren moeten vinden om de chemie die we hebben te verbeteren, ' zei Su.
Een paper gebaseerd op het onderzoek, "Een selectieregel voor hydrofluorether-elektrolyt-co-oplosmiddel:het vaststellen van een lineaire vrije-energierelatie in lithium-zwavelbatterijen, " verscheen in het nummer van 13 mei van Angewandte Chemie .
 Nieuwe synthesemethode opent mogelijkheden voor organische elektronica
Nieuwe synthesemethode opent mogelijkheden voor organische elektronica Nanokristallijne materialen met verminderde zuurstof vertonen verbeterde prestaties
Nanokristallijne materialen met verminderde zuurstof vertonen verbeterde prestaties Onderzoek doen:ladingsstroom door eiwitten onderzoeken
Onderzoek doen:ladingsstroom door eiwitten onderzoeken Bio-ingenieurs creëren een weg naar gepersonaliseerde geneeskunde
Bio-ingenieurs creëren een weg naar gepersonaliseerde geneeskunde Een snel en goedkoop apparaat om virussen op te vangen en te identificeren
Een snel en goedkoop apparaat om virussen op te vangen en te identificeren
 Wat wordt er gedaan om de zandkat te redden?
Wat wordt er gedaan om de zandkat te redden?  Wetenschappers komen samen om ozon te bestuderen, een atmosferisch mysterie in de buurt van Lake Michigan
Wetenschappers komen samen om ozon te bestuderen, een atmosferisch mysterie in de buurt van Lake Michigan Studie toont de kosten van ontbossing in Cambodja
Studie toont de kosten van ontbossing in Cambodja De droge gebieden van Afrika krijgen meer steun. Hoe u hier het beste van kunt maken?
De droge gebieden van Afrika krijgen meer steun. Hoe u hier het beste van kunt maken? Niet te rechtvaardigen:nieuw rapport laat zien hoe de gasexpansie van de natie Australiërs in gevaar brengt
Niet te rechtvaardigen:nieuw rapport laat zien hoe de gasexpansie van de natie Australiërs in gevaar brengt
Hoofdlijnen
- Warme wateren in het noordwesten trekken paaiende vissen naar het noorden
- Onderzoekers verwachten dat nieuwe vispassage de trekvispopulaties zal herstellen
- Wat gebeurt er met plantaardige en dierlijke cellen wanneer ze worden geplaatst in hypertone, hypotone en isotone omgevingen?
- Waar komt collageen vandaan?
- Volledig diagram van het menselijk lichaam
- Chinese wetenschappers onthullen een nieuwe signaalroute voor koude tolerantie in rijst
- High School Biology Topics
- Hoe Rigor Mortis te onderscheiden van een Cadaveric Spasm
- Onderzoeker koppelt zalmseks aan geologische verandering
- Bruggen bouwen tussen atomen en hoogwaardige katalysatoren maken

- Het periodiek systeem in een wetenschappelijke rekenmachine laden

- Ontdekking van een nieuw kandidaat-geneesmiddel om effectieve behandelingen voor hersenaandoeningen te ontwikkelen
- Een opschaalbare nanoporeuze membraancentrifuge voor ontzilting door omgekeerde osmose zonder vervuiling

- Hoeveel pot in die brownie? Chocolade kan tests afwerpen

 Onderzoek heeft tot doel tweetalige leerders begrijpend lezen te stimuleren
Onderzoek heeft tot doel tweetalige leerders begrijpend lezen te stimuleren PayPal koopt betalingsstart iZettle voor $ 2,2 miljard
PayPal koopt betalingsstart iZettle voor $ 2,2 miljard Wat is olie boren?
Wat is olie boren?  Berekening van velddiameter
Berekening van velddiameter Biocompatibele TeSex-nanolegeringen voor PT/PA/CT/PET-beeldgestuurde NIR-II-fotothermische therapie
Biocompatibele TeSex-nanolegeringen voor PT/PA/CT/PET-beeldgestuurde NIR-II-fotothermische therapie Aerosoldeeltjes koelen het klimaat minder af dan we dachten
Aerosoldeeltjes koelen het klimaat minder af dan we dachten De gids voor het maken van biomoleculaire films
De gids voor het maken van biomoleculaire films Onze reacties op geur onthullen onze politieke houding
Onze reacties op geur onthullen onze politieke houding
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | German | Dutch | Danish | Swedish | Norway |

-
Wetenschap © https://nl.scienceaq.com

