
Wetenschap
Zoutzuur versus azijnzuur:inzicht in de zuurgraad en waterstofionen
Dit is waarom:
* Sterk zuur versus zwak zuur: Zoutzuur is een sterk zuur, wat betekent dat het volledig ioniseert in water, waarbij alle waterstofionen vrijkomen. Azijnzuur is een zwak zuur, wat betekent dat het slechts gedeeltelijk ioniseert in water, waardoor minder waterstofionen vrijkomen.
* Ionisatie:
* HCl (aq) → H+ (aq) + Cl- (aq)
* CH3COOH (aq) ⇌ H+ (aq) + CH3COO- (aq)
* Concentratie: Zelfs als beide zuren geconcentreerd zijn, resulteert de volledige ionisatie van HCl in een veel hogere concentratie H+-ionen vergeleken met de gedeeltelijke ionisatie van azijnzuur.
Daarom heeft geconcentreerd zoutzuur een hogere zuurgraad en een grotere concentratie waterstofionen vergeleken met azijnzuur.
 Beschrijf de vier kwantumgetallen die worden gebruikt om een elektron in een atoom te karakteriseren
Beschrijf de vier kwantumgetallen die worden gebruikt om een elektron in een atoom te karakteriseren  Wat vormt de kern van atoom?
Wat vormt de kern van atoom?  Veel voorkomende alkalische stoffen in uw huis:gebruik en veiligheid
Veel voorkomende alkalische stoffen in uw huis:gebruik en veiligheid  Waar is de speciale functie die de familienaam en chemische reactiviteit van organische verbinding bepaalt die het heeft gevonden?
Waar is de speciale functie die de familienaam en chemische reactiviteit van organische verbinding bepaalt die het heeft gevonden?  Wat is de formule voor ZnCl2?
Wat is de formule voor ZnCl2?
Hoofdlijnen
- Nieuwe bevindingen uit onderzoek naar kunstmatige selectie wijzen op een bedreiging voor mariene omgevingen
- Wat hebben dierencellen die plant niet?
- Wie stelt wetenschappelijke vragen?
- Welk proces helpt het organisme de kans op overleving te vergroten?
- Cellulaire ademhaling versus fermentatie:belangrijkste verschillen verklaard
- Wat is een belangrijk verschil tussen een dierencel en een plantencel?
- Twee grote delen van een cel?
- Wat is de DNA -polymerase -rol bij replicatie?
- Waarom extraheren we DNA?
- Elektronische vaste stof kan de CO2-uitstoot in koelkasten en airconditioners verminderen

- Het spliceosoom - nu beschikbaar in hoge definitie
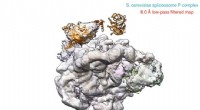
- De eerste ontdekking ter wereld kan de nieuwe groene ammoniakeconomie voeden

- Noedels verrijkt met voedingsvezels door geavanceerde technologie blijven lekker
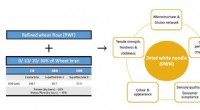
- Onderzoekers ontwikkelen materialen om geneesmiddelen uit afvalwater te verwijderen
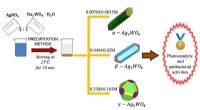
 Totale synthese van cotylenine A voor een nieuw geneesmiddel tegen kanker zonder bijwerkingen
Totale synthese van cotylenine A voor een nieuw geneesmiddel tegen kanker zonder bijwerkingen Hoe lekker is jouw nieuwjaarsbubbel? Luister goed
Hoe lekker is jouw nieuwjaarsbubbel? Luister goed Graphenes Big Mac maakt nieuwe generatie chips
Graphenes Big Mac maakt nieuwe generatie chips Astronaut Michael Collins, Apollo 11 piloot, dood aan kanker
Astronaut Michael Collins, Apollo 11 piloot, dood aan kanker Klimaatgedreven evolutie in bomen verandert hun ecosystemen
Klimaatgedreven evolutie in bomen verandert hun ecosystemen NASA test waarnemingsvermogen op de koraalriffen van Hawaï
NASA test waarnemingsvermogen op de koraalriffen van Hawaï Waarom rivieren belangrijk zijn voor de mondiale koolstofcyclus
Waarom rivieren belangrijk zijn voor de mondiale koolstofcyclus  Californische bosbranden hebben NorCals Air tot de ergste ter wereld gemaakt
Californische bosbranden hebben NorCals Air tot de ergste ter wereld gemaakt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

