
Wetenschap
Metaalcarbonylbinding:Sigma-donatie en backbonding uitgelegd
De aard van binding in metaalcarbonylen
Metaalcarbonylen zijn fascinerende verbindingen die een uniek soort binding vertonen. De kern van deze binding is een synergetische interactie tussen het metaal en de koolmonoxide (CO)-ligand. Hier is een overzicht:
1. Sigma-donatie:
* CO treedt op als sigmadonor , waarbij de elektronendichtheid van het enige paar op het koolstofatoom wordt gedoneerd aan een lege d-orbitaal van het metaal. Dit vormt een σ-binding tussen het metaal en het koolstofatoom.
2. Pi-backbonding:
* Het metaal schenkt op zijn beurt de elektronendichtheid van een gevulde d-orbitaal terug aan de antibindende π*-orbitaal van de CO-ligand. Dit vormt een π-binding en wordt π backbonding genoemd .
3. Synergie en gevolgen:
* Deze synergetische interactie , waarbij zowel de sigma-donatie als de pi-backbonding bijdragen aan de algehele bindingssterkte, is cruciaal voor de stabiliteit van metaalcarbonylen.
* Pi-backbonding verzwakt de C-O-binding in CO, wat leidt tot een langere C-O-binding en een lagere CO-rekfrequentie waargenomen bij IR-spectroscopie.
* Deze backbonding draagt ook bij aan de elektronegativiteit van het metaal , waardoor het meer elektronendeficiënt wordt.
4. Factoren die de hechting beïnvloeden:
* De mate van backbonding wordt beïnvloed door de volgende factoren:
* De elektronegativiteit van metaal: Meer elektronegatieve metalen (bijvoorbeeld Ni, Co) vertonen een sterkere rugbinding.
* Oditietoestand van metaal: Hogere oxidatietoestanden (meer positieve lading) leiden tot zwakkere backbonding.
* Het elektronenzuigende vermogen van Ligand: Elektronenzuigende groepen op het CO-ligand verminderen de backbonding.
5. Voorbeelden:
* Nikkeltetracarbonyl (Ni(CO)₄): Dit molecuul heeft een sterke rugbinding vanwege de lage elektronegativiteit van Ni en de afwezigheid van elektronenzuigende groepen.
* Chroomhexacarbonyl (Cr(CO)₆): Dit molecuul heeft een zwakkere backbinding vergeleken met Ni(CO)₄ vanwege de hogere elektronegativiteit van Cr en het grotere aantal CO-liganden.
6. Belang:
* Het begrijpen van bindingen in metaalcarbonylen is om verschillende redenen belangrijk:
* Reactiviteit voorspellen: Backbonding beïnvloedt de reactiviteit van metaalcarbonylen.
* Katalysatorontwerp: Metaalcarbonylen worden vaak gebruikt als katalysatoren bij organische reacties.
* Coördinatiechemie: Metaalcarbonylen zijn essentiële componenten in veel coördinatiecomplexen.
Samenvattend is de binding in metaalcarbonylen een complex samenspel van sigma-donatie en pi-backbonding. Deze synergetische interactie is cruciaal voor de stabiliteit van deze verbindingen en beïnvloedt hun reactiviteit en toepassingen.
 Hoe sloppenwijken veerkrachtiger kunnen worden tegen de klimaatverandering
Hoe sloppenwijken veerkrachtiger kunnen worden tegen de klimaatverandering  Hoe ongunstige abiotische en biotische factoren een soort beïnvloeden
Hoe ongunstige abiotische en biotische factoren een soort beïnvloeden  Wat is het verschil tussen vuil en stof?
Wat is het verschil tussen vuil en stof?  ISS-sensoren tonen terrestrische gammaflits- en ionosferische UV-emissies aangespoord door bliksem
ISS-sensoren tonen terrestrische gammaflits- en ionosferische UV-emissies aangespoord door bliksem Wat is een subtropische storm en hoe verschilt deze van een tropisch of extratropisch systeem?
Wat is een subtropische storm en hoe verschilt deze van een tropisch of extratropisch systeem?
Hoofdlijnen
- Is er een relatie tussen voedsel en uw bloedtype?
- Welk enzym is nodig om transcriptie te laten plaatsvinden?
- Scented Cleaning Products: The New Smoking?
- Wat is een proces door welke cellen in structuur veranderen?
- Wat is de enige flagellated cel in het lichaam?
- Welke kenmerken van eukaryotische organismen?
- Voor welke aspecten van het leven worden verklaard door evolutie?
- Welke theorie verklaart waarom de populatie in de loop van de tijd kan worden gewijzigd?
- Herten breiden zich uit naar het noorden, en dat is niet goed voor kariboes:wetenschappers evalueren de redenen waarom
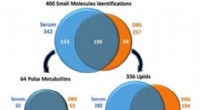
- Bij longitudinaal onderzoek gedroogde bloedvlekmonsters spelen een rol
- Slimme diëlektrische elastomeren voor zelfherstellende zachte robots

- Een nieuwe manier om MXene-films te maken die elektromagnetische interferentie blokkeren

- Wetenschappers ontwikkelen nieuwe, goedkope tool voor het detecteren van bacteriën in voedsel en water

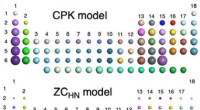
- Het onzichtbare visualiseren:een nieuw model om de interpretatie van moleculaire beelden met atomaire resolutie te vergemakkelijken
 Welke energietransfers worden gebruikt in de elektrische spoel van een plintverwarming?
Welke energietransfers worden gebruikt in de elektrische spoel van een plintverwarming?  Hoe klimaatverandering ervoor kan zorgen dat catastrofale weersystemen langer blijven hangen
Hoe klimaatverandering ervoor kan zorgen dat catastrofale weersystemen langer blijven hangen Wat is donkere energie? Binnen ons versnellende, uitdijende universum
Wat is donkere energie? Binnen ons versnellende, uitdijende universum  NASA's Aqua-satelliet toont windschering die tropische cycloon Riley beïnvloedt
NASA's Aqua-satelliet toont windschering die tropische cycloon Riley beïnvloedt Verkeersborden voor immuunafweercellen
Verkeersborden voor immuunafweercellen Welk object in de lucht produceert licht?
Welk object in de lucht produceert licht?  Exponenten op een wetenschappelijke rekenmachine gebruiken
Exponenten op een wetenschappelijke rekenmachine gebruiken Hoeveel atomen zijn er in 0,308 mol 13C?
Hoeveel atomen zijn er in 0,308 mol 13C?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

