
Wetenschap
Waterstofbinding versus polaire bindingen:welke is sterker?
* Waterstofbinding is een specifiek type intermoleculaire kracht . Het is de aantrekkingskracht tussen een waterstofatoom dat covalent gebonden is aan een zeer elektronegatief atoom (zoals zuurstof, stikstof of fluor) en een elektronenpaar op een ander elektronegatief atoom.
* Polaire binding verwijst naar een covalente binding waarbij de elektronen ongelijk verdeeld zijn tussen twee atomen vanwege verschillen in elektronegativiteit. Hierdoor ontstaat er een dipoolmoment binnen het molecuul.
Dus, wat is sterker?
* Polaire bindingen zijn inherent sterker dan waterstofbruggen. Ze zijn het feitelijk delen van elektronen binnen een molecuul, waardoor een sterkere kracht ontstaat.
* Waterstofbruggen zijn nog steeds belangrijk! Hoewel ze zwakker zijn dan polaire bindingen, spelen ze een cruciale rol in veel biologische processen, zoals het bij elkaar houden van DNA-strengen en het bepalen van de structuur van eiwitten.
Zie het zo:
* Stel je een groep mensen voor die elkaars hand vasthouden (waterstofbruggen). Ze kunnen relatief eenvoudig uit elkaar worden getrokken.
* Stel je nu voor dat twee mensen elkaar stevig vasthouden (polaire banden). Het kost meer moeite om ze te scheiden.
Belangrijkste afhaalpunten:
* Polaire bindingen zijn sterker binnen een molecuul.
* Waterstofbruggen zijn zwakkere maar belangrijke krachten tussen moleculen.
 Hoe verhoudt de atoomstraal van broom zich tot chloor?
Hoe verhoudt de atoomstraal van broom zich tot chloor?  Efficiënte katalysator op basis van titanium gebruikt om PEF te produceren, biobased alternatief voor PET
Efficiënte katalysator op basis van titanium gebruikt om PEF te produceren, biobased alternatief voor PET Hoe gebruiken farmaceutische producten wetenschappelijke notatie?
Hoe gebruiken farmaceutische producten wetenschappelijke notatie?  Een materiaal met een bijzondere twist:2-D molybdeendiselenidekristal
Een materiaal met een bijzondere twist:2-D molybdeendiselenidekristal Welk element wordt beschouwd als de basis voor het maken van organische verbindingen?
Welk element wordt beschouwd als de basis voor het maken van organische verbindingen?
 Grootse ideeën, wereldwijde nagalm:Grand Canyon op zijn 6 miljoenste verjaardag
Grootse ideeën, wereldwijde nagalm:Grand Canyon op zijn 6 miljoenste verjaardag Diepe mantelchemie-verrassing:koolstofgehalte niet uniform
Diepe mantelchemie-verrassing:koolstofgehalte niet uniform Kunnen verschillende natuurkrachten elkaar beïnvloeden?
Kunnen verschillende natuurkrachten elkaar beïnvloeden?  Aqua-satelliet ziet orkaan Michael sterker worden
Aqua-satelliet ziet orkaan Michael sterker worden NASA's Terra-satelliet analyseert Caribische tropische depressie 14
NASA's Terra-satelliet analyseert Caribische tropische depressie 14
Hoofdlijnen
- Wat zijn dragerseiwitten?
- Wat is de wetenschappelijke notatie van menselijk DNA?
- Welk proces voeren Ribosomes uit?
- Wat is het proces van het maken van een kopie -DNA voor doel -eiwitten?
- Breng de meeste eiwit- en aminozurenhormonen hun effect teweeg door interactie met onze genen?
- Hoeveel chromosoom zit er in een ei?
- Wat zijn de verschillen tussen autochtone en allochtone micro -organismen in aquatische omgevingen?
- Welke micro -organismen zijn niet schadelijk?
- Opnieuw kijken naar het uitsterven van de Centinela Ridge:nieuw onderzoek toont aan dat de meeste ‘uitgestorven’ soorten nog steeds overleven
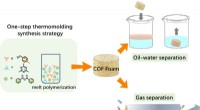
- Gebruik van smeltpolymerisatie om robuust covalent organisch raamwerkschuim te fabriceren
- Coördinatiepolymeren met tot 99,99% antibacteriële efficiëntie

- Nanodiamanten als fotokatalysatoren

- Wetenschappers onderzoeken macrocyclische peptiden als nieuwe medicijnsjablonen

- Onderzoekers onderzoeken ontstekingsremmende activiteit van curcumine

 Waar is de hoogste bergtop op aarde gevestigd?
Waar is de hoogste bergtop op aarde gevestigd?  Een niet -geïdentificeerd mineraal dat zachter is dan calciet vertoont een metalen glans en kubieke splitsing?
Een niet -geïdentificeerd mineraal dat zachter is dan calciet vertoont een metalen glans en kubieke splitsing?  Welke plantencelstructuren lijken te ontbreken in de cellen van een uienlamp?
Welke plantencelstructuren lijken te ontbreken in de cellen van een uienlamp?  Wat dient als controle voor celmetabolisme en reproductie?
Wat dient als controle voor celmetabolisme en reproductie?  Is Francium een goede warmtegeleider?
Is Francium een goede warmtegeleider?  Amerikanen samenbrengen over de kwestie van betaalbare huisvesting
Amerikanen samenbrengen over de kwestie van betaalbare huisvesting Waar hangen alle organismen in een voedselweb uiteindelijk van?
Waar hangen alle organismen in een voedselweb uiteindelijk van?  Is kalkwater een zuur of alkali?
Is kalkwater een zuur of alkali?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

