
Wetenschap
Polariteit begrijpen:waarom water polair is en kooldioxide niet-polair
Dit is waarom:
Kooldioxide (CO₂)
* Structuur: CO₂ heeft een lineaire structuur. Het koolstofatoom bevindt zich in het midden en de twee zuurstofatomen bevinden zich aan weerszijden.
* Elektronegativiteit: Zuurstof is elektronegatiever dan koolstof. Dit betekent dat zuurstofatomen elektronen sterker aantrekken, waardoor er een lichte negatieve lading ontstaat rond de zuurstofatomen en een lichte positieve lading rond het koolstofatoom.
* Symmetrie: De twee zuurstofatomen trekken de elektronen gelijkmatig in tegengestelde richtingen. Hierdoor ontstaat een symmetrische verdeling van de lading en heeft het molecuul geen netto dipoolmoment . Daarom wordt CO₂ als niet-polair beschouwd .
Water (H₂O)
* Structuur: Water heeft een gebogen of V-vormige structuur. Het zuurstofatoom bevindt zich in het midden, met twee waterstofatomen onder een hoek.
* Elektronegativiteit: Zuurstof is elektronegatiever dan waterstof. Hierdoor ontstaat een gedeeltelijke negatieve lading op het zuurstofatoom en gedeeltelijke positieve lading op de waterstofatomen.
* Asymmetrie: De gebogen structuur en de ongelijke verdeling van de lading zorgen ervoor dat de twee waterstofatomen de negatieve lading van de zuurstof niet opheffen. Dit resulteert in een netto dipoolmoment , waardoor water een polair molecuul wordt .
Samengevat:
* CO₂ is niet-polair vanwege de lineaire structuur en de symmetrische ladingsverdeling.
* H₂O is polair vanwege de gebogen structuur en de ongelijke verdeling van de lading, waardoor een netto dipoolmoment ontstaat.
 Onderzoek laat zien hoe sociale relaties vogelkoppels transformeren
Onderzoek laat zien hoe sociale relaties vogelkoppels transformeren  Rechtbank beveelt verbod op schadelijke pesticiden, zegt dat EPA de wet heeft overtreden
Rechtbank beveelt verbod op schadelijke pesticiden, zegt dat EPA de wet heeft overtreden Onderzoek vindt kustwegen onder nieuwe bedreiging door stijgende zeespiegel
Onderzoek vindt kustwegen onder nieuwe bedreiging door stijgende zeespiegel Het dekken van de vuurterreur in het verloren paradijs van Californië
Het dekken van de vuurterreur in het verloren paradijs van Californië Amerikanen gebruiken elke dag 500 miljoen rietjes. Zou je beloven om Strawless te gaan?
Amerikanen gebruiken elke dag 500 miljoen rietjes. Zou je beloven om Strawless te gaan?
Hoofdlijnen
- Wat zit er in elke cel in je lichaam?
- Wat zijn de lange moleculen van DNA die meestal worden gevonden in paren die worden genoemd?
- Statistische modellering helpt visserijbeheerders invasieve soorten te verwijderen
- Welke soorten weefsels vormen het skeletsysteem?
- Wat zijn alle wetenschapswoorden die beginnen met C?
- Wat zijn de ingrediënten van het menselijk lichaam?
- Over hoeveel verschillende soorten organismen hebben wetenschappers tot nu toe ontdekt?
- Hoe denken wetenschappers dat symbiotische relaties zijn geëvolueerd?
- Waar kan een eencellig organisme in leven?
- Nieuw, gevoeliger sensor voor het evalueren van de veiligheid van geneesmiddelen
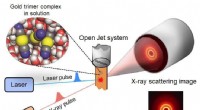
- Elk moment van ultrasnelle chemische binding vastgelegd op film
- Van melkeiwit, een plastic schuim dat beter wordt in een moeilijke omgeving

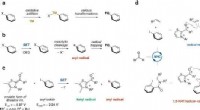
- Arylradicaalvorming door splitsing van arylhalogenidebindingen door een N-heterocyclische carbeenkatalysator
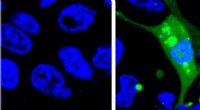
- Snelle tests voor vroege diagnose van hartaanvallen en identificatie van sepsis

 Als een auto met 26 mijl per uur reist, wat zijn snelheid in lilometers uur?
Als een auto met 26 mijl per uur reist, wat zijn snelheid in lilometers uur?  Hoeveel water is nodig om zout op te lossen?
Hoeveel water is nodig om zout op te lossen?  Potentiële energie en kinetische energie definiëren?
Potentiële energie en kinetische energie definiëren?  Niet klaar voor SAT? Teen's website kan het antwoord zijn
Niet klaar voor SAT? Teen's website kan het antwoord zijn  Wat zijn de producten van een hydrolyse ATP?
Wat zijn de producten van een hydrolyse ATP?  Welke planeet reist rond de zon met de laagste snelheid?
Welke planeet reist rond de zon met de laagste snelheid?  Uit onderzoek blijkt dat mannelijke genen behouden blijven na het verlies van mannetjes bij wandelende takken
Uit onderzoek blijkt dat mannelijke genen behouden blijven na het verlies van mannetjes bij wandelende takken  Waarom mechanische golf een medium vereist om energie over te dragen?
Waarom mechanische golf een medium vereist om energie over te dragen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

