
Wetenschap
Hoe batterijen werken:chemische reacties en elektrische stroom
Hier is hoe het werkt:
* Elektrolyt: Een batterij bevat een elektrolyt, een oplossing die elektriciteit geleidt.
* Elektroden: De elektrolyt staat in contact met twee elektroden, meestal gemaakt van verschillende metalen.
* Chemische reactie: Er vindt een chemische reactie plaats tussen de elektrolyt en de elektroden, waardoor elektronen van de ene elektrode naar de andere stromen.
* Elektrische stroom: Deze elektronenstroom creëert een elektrische stroom die kan worden gebruikt om apparaten van stroom te voorzien.
Typen batterijen:
Er zijn verschillende soorten batterijen, die elk verschillende chemische reacties gebruiken:
* Primaire batterijen: Dit zijn wegwerpbatterijen die niet kunnen worden opgeladen. Voorbeelden zijn onder meer alkalische batterijen en koolstof-zinkbatterijen.
* Secundaire batterijen: Dit zijn oplaadbare batterijen die meerdere keren gebruikt kunnen worden. Voorbeelden hiervan zijn loodzuurbatterijen (gebruikt in auto's), lithium-ionbatterijen (gebruikt in telefoons en laptops) en nikkel-cadmiumbatterijen.
Andere apparaten:
Hoewel batterijen het meest voorkomende voorbeeld zijn, gebruiken andere apparaten ook chemische reacties om elektriciteit op te wekken:
* Brandstofcellen: Deze apparaten gebruiken chemische reacties tussen een brandstof (zoals waterstof) en een oxidatiemiddel (zoals zuurstof) om elektriciteit te produceren.
* Elektrochemische sensoren: Deze apparaten gebruiken chemische reacties om specifieke stoffen te detecteren en te meten.
* Elektrolyse: Bij dit proces wordt elektriciteit gebruikt om chemische reacties aan te sturen, bijvoorbeeld om water te ontleden in waterstof en zuurstof.
Laat het me weten als je meer wilt weten over een specifiek type batterij of apparaat!
 VK publiceert plannen om het vervoer tegen het midden van de eeuw koolstofarm te maken
VK publiceert plannen om het vervoer tegen het midden van de eeuw koolstofarm te maken Het vochtproces dat wordt vrijgelaten uit de bladerenbomen en planten in de lucht?
Het vochtproces dat wordt vrijgelaten uit de bladerenbomen en planten in de lucht?  Schone stroom is niet genoeg
Schone stroom is niet genoeg Ontdekken hoe rivierwater in de zee wordt gemengd, kan helpen bij het in kaart brengen van de klimaatverandering
Ontdekken hoe rivierwater in de zee wordt gemengd, kan helpen bij het in kaart brengen van de klimaatverandering  Wat is het verschil tussen Caves Rock Shelter and Houses?
Wat is het verschil tussen Caves Rock Shelter and Houses?
Hoofdlijnen
- Wat is recombinante DNA -technologie?
- Welke celstructuur wordt gebruikt om zich voor te bereiden op depolarisatie?
- Hoe cellen nauwkeurige DNA-replicatie garanderen:belangrijke mechanismen uitgelegd
- Duurzaamheid van visserij gekoppeld aan genderrollen onder handelaren
- Leg uit waarom biomen niet gelijkmatig worden verdeeld over de wereld?
- Wat is organel dat cellulaire ademhaling uitvoert een fotosynthese?
- Wat is de generieke term voor een structuur in cel die op zichzelf een afzonderlijk functiecompartiment vormen?
- Wat zijn organismen die hun eigen voedsel produceren?
- Wat de levendige pigmenten van vogelveren ons kunnen leren over hoe evolutie werkt
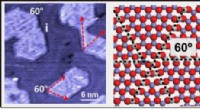
- Atomaire defectlijnen onderdrukken deactivering van ijzeroxidekatalysatoren
- Scherm kan betere veiligheidstests bieden voor nieuwe chemicaliën
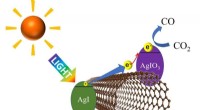
- Zichtbaar licht gebruiken om koolstofdioxide efficiënt af te breken
- Een onverwacht werkingsmechanisme voor een antilichaam

- Make like a leaf:onderzoekers ontwikkelen methode om koolstofdioxide om te zetten

 Wat bevat grotere OH-ionen, een zuur of een base?
Wat bevat grotere OH-ionen, een zuur of een base?  Hoe zegt de wetenschap dat het menselijk leven begon?
Hoe zegt de wetenschap dat het menselijk leven begon?  Team ontwikkelt wiskundige technieken om de rekenefficiëntie in de kwantumchemie te verbeteren
Team ontwikkelt wiskundige technieken om de rekenefficiëntie in de kwantumchemie te verbeteren Hoe vaak draaien de planeten in één aardjaar om de zon?
Hoe vaak draaien de planeten in één aardjaar om de zon?  Boeing zegt dat 737 MAX naar verwachting in januari weer zal vliegen
Boeing zegt dat 737 MAX naar verwachting in januari weer zal vliegen Wanneer een object door de lucht versnelt, zijn de krachten van stuwkracht en weerstand dan in evenwicht?
Wanneer een object door de lucht versnelt, zijn de krachten van stuwkracht en weerstand dan in evenwicht?  Gebruikt energie uit voedsel om hoge verbindingen te maken?
Gebruikt energie uit voedsel om hoge verbindingen te maken?  Welke elementen heeft de koolstoffamilie 4 valentie -elektronen?
Welke elementen heeft de koolstoffamilie 4 valentie -elektronen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

