
Wetenschap
Inzicht in de binding van watermoleculen:covalente bindingen en polariteit
* Elektronen delen: Elk waterstofatoom heeft één elektron in de buitenste schil, terwijl zuurstof er zes heeft. Om een stabiele configuratie te bereiken, delen ze elektronen. Het zuurstofatoom deelt één elektron met elk waterstofatoom en vormt twee covalente bindingen.
* Polariteit: Zuurstof is elektronegatiever dan waterstof, wat betekent dat het de gedeelde elektronen dichter naar zich toe trekt. Hierdoor ontstaat een gedeeltelijke negatieve lading op het zuurstofatoom en gedeeltelijke positieve lading op de waterstofatomen. Dit maakt het watermolecuul polair , met een positief einde en een negatief einde.
De aantrekkingskracht tussen de gedeeltelijk positieve waterstofatomen van één watermolecuul en het gedeeltelijk negatieve zuurstofatoom van een ander watermolecuul wordt een waterstofbrug genoemd.
Waterstofbruggen zijn zwakker dan covalente bindingen, maar ze zijn nog steeds belangrijk omdat ze:
* Houd watermoleculen bij elkaar: Hierdoor krijgt water een hoge oppervlaktespanning en kan het bij kamertemperatuur als vloeistof bestaan.
* Laat water veel stoffen oplossen: De polariteit van watermoleculen helpt hen ionische verbindingen af te breken en polaire moleculen aan te trekken.
* Speel een cruciale rol in biologische processen: Waterstofbruggen zijn essentieel voor het behoud van de structuur van eiwitten, DNA en andere biologische moleculen.
 Henri Becquerel's ontdekking van radioactiviteit:een fotografisch plaatexperiment
Henri Becquerel's ontdekking van radioactiviteit:een fotografisch plaatexperiment  Wie zei dat de meeste van een atomenmassa zich in het kernatoom bevindt?
Wie zei dat de meeste van een atomenmassa zich in het kernatoom bevindt?  Wat zijn enkele manieren om vaste materialen te veranderen?
Wat zijn enkele manieren om vaste materialen te veranderen?  Mengsels versus verbindingen:waarom de samenstelling varieert
Mengsels versus verbindingen:waarom de samenstelling varieert  Eiwit dat chemische oorlogsvoering kan voorkomen, gemaakt
Eiwit dat chemische oorlogsvoering kan voorkomen, gemaakt
Hoofdlijnen
- Wat is Bacteriuria?
- Wat zijn de drie componenten die nucleïnezuren vormen?
- Wat is een evolutionaire boom, hoe anders dan een stamboom?
- Wat is de klier in de hersenen die gereguleerd door licht?
- Longhornteek voor het eerst ontdekt in het noorden van Missouri
- Welk type opvolging veroorzaakt de biotische componenten die een gemeenschap veroorzaakt?
- Verband tussen nummervolgorde en ritmische timing bij zangvogels
- Hoe de cellen van planten, dieren en eencellige organismen te vergelijken
- Wat is een wetenschapsdefinitie voor mond?
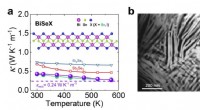
- Extreem lage thermische geleidbaarheid in 1-D zachte kettingstructuur
- Wat doet een chemische stof? Misvattingen over scheikunde aanpakken

- Computerwetenschappers en materiaalonderzoekers werken samen om staalclassificatie te optimaliseren

- Nieuwe tool kan bloedinfecties snel behandelen
- Ontwikkeling van een zeer duurzame enkel-atomige katalysator met behulp van industriële luchtbevochtiger

 Hoe kan de temperatuur van de oven worden gemeten?
Hoe kan de temperatuur van de oven worden gemeten?  Wat is de Griekse wortel van woordgeografie?
Wat is de Griekse wortel van woordgeografie?  Kussende insecten, vector voor de ziekte van Chagas, voor het eerst met succes gen-editing
Kussende insecten, vector voor de ziekte van Chagas, voor het eerst met succes gen-editing  Zijn de grootste vulkanen op aarde per volume hotspots gevonden tektonische spreidingscentra of oceanische transformatiefouten?
Zijn de grootste vulkanen op aarde per volume hotspots gevonden tektonische spreidingscentra of oceanische transformatiefouten?  Efficiëntere optische kwantumpoorten
Efficiëntere optische kwantumpoorten Afbeelding:lancering van SpaceX Falcon 9 en Dragon vanaf lanceercomplex 39A
Afbeelding:lancering van SpaceX Falcon 9 en Dragon vanaf lanceercomplex 39A Hoe werd het sterrenbeeld Leo ontdekt?
Hoe werd het sterrenbeeld Leo ontdekt?  Welke kenmerken delen de meeste bacteriën?
Welke kenmerken delen de meeste bacteriën?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

