
Wetenschap
Welk zuur is een sterke elektrolyt A. zwavelzuur B. azijnzuur C. mierenzuur D. citroenzuur?
Het juiste antwoord is A. zwavelzuur.
Zwavelzuur is een sterke elektrolyt omdat het volledig dissocieert in zijn ionen wanneer het in water wordt opgelost. Dit betekent dat alle zwavelzuurmoleculen uiteenvallen in waterstofionen (H+) en sulfaationen (SO42-). Hierdoor kan zwavelzuur elektriciteit heel goed geleiden.
Azijnzuur, mierenzuur en citroenzuur zijn allemaal zwakke elektrolyten. Dit betekent dat ze slechts gedeeltelijk dissociëren in hun ionen wanneer ze in water worden opgelost. Als gevolg hiervan geleiden deze zuren elektriciteit niet zo goed als zwavelzuur.
 Nieuwe manier om influenza A-virus te identificeren licht op wanneer specifieke virusdoelen aanwezig zijn
Nieuwe manier om influenza A-virus te identificeren licht op wanneer specifieke virusdoelen aanwezig zijn Wetenschappers ontrafelen de mysteries van onomkeerbaarheid in elektrochrome dunne films
Wetenschappers ontrafelen de mysteries van onomkeerbaarheid in elektrochrome dunne films Wat is een molaire massa en hoeveel atomen zitten er in 1 mol van iets?
Wat is een molaire massa en hoeveel atomen zitten er in 1 mol van iets?  Wat is een fysieke eigenschap van een gigantische covalente structuur?
Wat is een fysieke eigenschap van een gigantische covalente structuur?  Hoeveel mol broomatomen in 1 mol gas Scheikundevraag heeft hulp nodig bij huiswerk?
Hoeveel mol broomatomen in 1 mol gas Scheikundevraag heeft hulp nodig bij huiswerk?
 Ian kan een catastrofale orkaan van categorie 4 worden. NASA overweegt raket op te bergen
Ian kan een catastrofale orkaan van categorie 4 worden. NASA overweegt raket op te bergen Klimaatverandering betekent langer opstijgen en minder passagiers per vliegtuig
Klimaatverandering betekent langer opstijgen en minder passagiers per vliegtuig Emissies van menselijke activiteit wijzigen de vorming van biogene secundaire organische aerosolen
Emissies van menselijke activiteit wijzigen de vorming van biogene secundaire organische aerosolen Onderzoeker bespreekt aanpak van wereldwijde klimaatverandering op regionale schaal
Onderzoeker bespreekt aanpak van wereldwijde klimaatverandering op regionale schaal Nieuwe gegevens verzamelen over atmosferische deeltjes voor stormvoorspelling en klimaatmodellen
Nieuwe gegevens verzamelen over atmosferische deeltjes voor stormvoorspelling en klimaatmodellen
Hoofdlijnen
- Hoe de kaken van het leven werken
- Hoe damselfish en myside garnalen naast elkaar bestaan in een wederzijds voordelige relatie
- Het belangrijkste orgaan in ons lichaam zijn de hersenen?
- Wat zou er met een voedselketen gebeuren als de populatie van één organisme zou toenemen?
- Waarom worden reuzenpanda’s zo klein geboren?
- Welke soorten schimmels?
- Wat is een brownfield?
- Waarom hebben zoveel van onze huisdieren overgewicht?
- Bijen zijn verbazingwekkend goed in het nemen van beslissingen – en ons computermodel legt uit hoe dat mogelijk is
- Een nieuw idee verbindt de synthese van klei en de oorsprong van het metabolisme

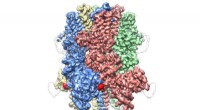
- Cryo-EM onthult kroonachtige structuur van eiwit dat verantwoordelijk is voor het reguleren van de bloedstroom
- Gecontroleerde fabricage van multimetalen bouwstenen voor hybride nanomaterialen

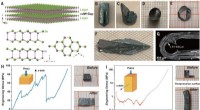
- Onderzoekers ontdekken dat kristallen van indiumselenide een uitzonderlijke flexibiliteit hebben
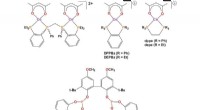
- Nieuw kobaltcomplex kan de kosten van hydroformylering verlagen
 Kreeftenvertering van microplastics kan de voedselketen verder vervuilen
Kreeftenvertering van microplastics kan de voedselketen verder vervuilen Maduro zegt dat Venezuela een injectie van $ 1 miljard krijgt van de verkoop van bitcoin
Maduro zegt dat Venezuela een injectie van $ 1 miljard krijgt van de verkoop van bitcoin Kan kunstmatige intelligentie volgens de wet als een persoon worden beschouwd?
Kan kunstmatige intelligentie volgens de wet als een persoon worden beschouwd? Magische handschoenen laten de veelgeprezen Braziliaanse pianist weer spelen
Magische handschoenen laten de veelgeprezen Braziliaanse pianist weer spelen Een transparant flexibel materiaal maken van zijde en nanobuisjes
Een transparant flexibel materiaal maken van zijde en nanobuisjes Lab-gekweekte pigmenten en voedselbijproducten:de toekomst van natuurlijke textielkleurstoffen
Lab-gekweekte pigmenten en voedselbijproducten:de toekomst van natuurlijke textielkleurstoffen Vergelijkbare toestanden van activiteit geïdentificeerd in superzware en stellaire zwarte gaten
Vergelijkbare toestanden van activiteit geïdentificeerd in superzware en stellaire zwarte gaten Apple prijst privacyfuncties van nieuwe besturingssystemen
Apple prijst privacyfuncties van nieuwe besturingssystemen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

