
Wetenschap
Kookpunten van gassen:verdamping en condensatie begrijpen
* Kookpuntdefinitie: Kookpunt is de temperatuur waarbij een vloeistof bij een bepaalde druk overgaat in een gas (damp).
* Gassen bevinden zich al in de dampfase: Gassen bevinden zich al in de gasfase bij normale temperaturen en drukken. Ze hoeven niet over te stappen van een vloeibare toestand.
* Condensatie: In plaats van een kookpunt hebben gassen een condensatiepunt , wat de temperatuur is waarbij ze overgaan van een gas naar een vloeistof.
Gassen kunnen echter een kritiek punt hebben:
* Kritisch punt: Dit is de temperatuur en druk waarboven een stof niet als vloeistof kan bestaan, ongeacht hoeveel druk er wordt uitgeoefend. Boven het kritieke punt bestaat de stof als een superkritische vloeistof, die eigenschappen heeft van zowel vloeistoffen als gassen.
Samengevat:
Hoewel gassen geen kookpunt hebben, hebben ze wel een condensatiepunt en een kritisch punt. Deze concepten helpen ons het gedrag van gassen bij verschillende temperaturen en drukken te begrijpen.
 Nieuw onderzoek laat zien hoe klimaatverandering de impact van rondwormen op graslanden kan beïnvloeden
Nieuw onderzoek laat zien hoe klimaatverandering de impact van rondwormen op graslanden kan beïnvloeden  Welk element komt het meest voor in levende wezens?
Welk element komt het meest voor in levende wezens?  Hoe beïnvloeden langzame anomalieën onder subductieplaten gigantische megathrust-aardbevingen?
Hoe beïnvloeden langzame anomalieën onder subductieplaten gigantische megathrust-aardbevingen? Fatsoenlijk leven voor iedereen hoeft de aarde niet te kosten
Fatsoenlijk leven voor iedereen hoeft de aarde niet te kosten De voordelen van het gebruik van de wetenschappelijke methode bij het bestuderen van milieuproblemen?
De voordelen van het gebruik van de wetenschappelijke methode bij het bestuderen van milieuproblemen?
Hoofdlijnen
- Hoe dicht is een cel? Onderzoekers hebben een manier bedacht om die vraag te beantwoorden
- Welk effect heeft de temperatuur op cellulaire enzymactiviteit?
- Levenslange bloedproductie is afhankelijk van honderden cellen die zich vóór de geboorte vormen
- Wat is een biosample?
- Menselijk genoom bevat hoeveel?
- Twee wetenschappers bestuderen gegevens die zijn verzameld tijdens een experiment en trekken verschillende conclusies. Hoe zou de wetenschappelijke gemeenschap hun meningsverschil aanpakken?
- Lang of kort? Dik dun? Onderzoek toont aan dat veel factoren de arm- en beenomvang beïnvloeden
- Robot ‘leert’ hoe te functioneren in menselijke omgevingen
- Is er zoiets als eiwitpil?
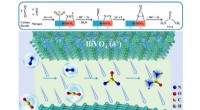
- Nieuwe katalysatoren verbeteren de efficiëntie van de ureumsynthese bij omgevingsomstandigheden
- Het AI-gestuurde initiatief dat de ontdekking van medicijnen voor de behandeling van COVID-19 versnelt

- Nieuwe synthetische route voor amanitine, een therapeutisch interessant paddenstoelentoxine

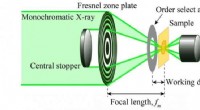
- Een scanning transmissie-röntgenmicroscoop voor analyse van chemische toestanden van lithium
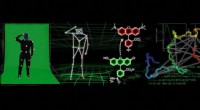
- Chemici ontwikkelen motion capture-achtige technologie voor het volgen van eiwitvorm
 Wat is de personificatiebetekenis van heldere bliksemflitsen die in de lucht dansten?
Wat is de personificatiebetekenis van heldere bliksemflitsen die in de lucht dansten?  The Biotic Factors voor Alpine Tundra
The Biotic Factors voor Alpine Tundra  Afgeleid door technologie? Microsoft probeert te helpen
Afgeleid door technologie? Microsoft probeert te helpen Heeft de Cotopaxi -vulkaan een natuurramp veroorzaakt?
Heeft de Cotopaxi -vulkaan een natuurramp veroorzaakt?  Geef 10 voorbeelden van stollingsgesteente.
Geef 10 voorbeelden van stollingsgesteente.  Hoe enzymen functioneren in chemische reacties?
Hoe enzymen functioneren in chemische reacties?  Wat zijn moleculen die opgeroepen zijn door enzymen die worden genoemd?
Wat zijn moleculen die opgeroepen zijn door enzymen die worden genoemd?  Op sensoren gebaseerde technologieën zijn veelbelovend om het zelfstandig leven van oudere vrouwen te ondersteunen
Op sensoren gebaseerde technologieën zijn veelbelovend om het zelfstandig leven van oudere vrouwen te ondersteunen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

