
Wetenschap
Energie die vrijkomt bij de lithium-waterreactie:berekening en uitleg
Reactie:
2 Li(s) + 2 H₂O(l) → 2 LiOH(aq) + H₂(g)
Berekening van de enthalpieverandering (ΔH):
Je moet de standaardvormingsenthalpieën (ΔHf°) opzoeken voor elke verbinding die bij de reactie betrokken is. Deze waarden zijn doorgaans te vinden in scheikundeboeken of online databases.
Hier is een vereenvoudigd voorbeeld met hypothetische ΔHf°-waarden (u moet de werkelijke waarden opzoeken):
* ΔHf° [LiOH(aq)] =-485 kJ/mol
* ΔHf° [H₂(g)] =0 kJ/mol (per definitie)
* ΔHf° [Li(s)] =0 kJ/mol (per definitie)
* ΔHf° [H₂O(l)] =-286 kJ/mol
De wet van Hess gebruiken:
ΔH =[Σ ΔHf° (producten)] - [Σ ΔHf° (reactanten)]
ΔH =[2 * (-485 kJ/mol) + 0] - [2 * 0 + 2 * (-286 kJ/mol)]
ΔH =-970 kJ/mol + 572 kJ/mol
ΔH =-398 kJ/mol
Belangrijke opmerking: Dit resultaat geldt voor de reactie van *twee* mol lithium. Om de energie per mol lithium te krijgen, deelt u door 2:
-398 kJ/mol / 2 =-199 kJ/mol
Daarom komt bij de reactie van lithium met water ongeveer 199 kJ energie per mol lithium vrij.
Veiligheid:
Houd er rekening mee dat deze reactie zeer krachtig is en waterstofgas produceert, dat brandbaar is. Ga altijd uiterst voorzichtig om met lithium en water en voer dit experiment nooit uit zonder de juiste veiligheidsuitrusting en toezicht.
 Hoeveel zintuigen heeft de mens?
Hoeveel zintuigen heeft de mens?  Nieuwe technologie vindt lang verborgen aardbevingen en mogelijke aanwijzingen over hoe aardbevingen evolueren
Nieuwe technologie vindt lang verborgen aardbevingen en mogelijke aanwijzingen over hoe aardbevingen evolueren Waarom is regenwoud zo belangrijk?
Waarom is regenwoud zo belangrijk?  Hoge uitstoot van broeikasgassen uit Siberische binnenwateren
Hoge uitstoot van broeikasgassen uit Siberische binnenwateren NASA's meerdere weergaven van orkaan Dorian vanuit de ruimte
NASA's meerdere weergaven van orkaan Dorian vanuit de ruimte
Hoofdlijnen
- Waarom kunnen twee soorten niet dezelfde niche bezetten?
- Wat veroorzaakt bacteriële vervuiling?
- Waarom zou een wetenschapper liever de lagere krachten van de lichtmicroscoop kunnen gebruiken, aspecten een unicellulair organisme waarnemen?
- In welke cel is er geen verdeling?
- Welke structuren in plantencellen vanen lichte energie om voedsel te produceren?
- Wat zijn niet -voorbeelden van evolutie?
- Ontbrekende schakel in het behoud van soorten:apothekers en scheikundigen kunnen het tij keren wat betreft het uitsterven van planten en dieren
- Wat voor soort organisme maakt het eigen voedsel?
- Nieuwe procedure voor snellere detectie van milieueffecten van zalmkwekerijen
- Biologische verwering begrijpen:hoe levende organismen ons landschap vormen

- Eiwit-gemodificeerde vaste elektrolyt interfase vorming en evolutie in Li-metaalbatterijen

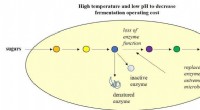
- Onderzoekers ontwikkelen sterkere microben om de bioproductie van brandstoffen te verbeteren, Chemicaliën
- Zijn antivitamines de nieuwe antibiotica?

- Eenvoudige vergelijking leidt tot het creëren van schone-energiekatalysatoren
 Hebben de banen van de meeste planeten excentriciteit bijna nul?
Hebben de banen van de meeste planeten excentriciteit bijna nul?  15, 000 wetenschappers in 184 landen waarschuwen voor negatieve wereldwijde milieutrends
15, 000 wetenschappers in 184 landen waarschuwen voor negatieve wereldwijde milieutrends Wat betekent het als twee organismen vele niveaus van classificatie delen?
Wat betekent het als twee organismen vele niveaus van classificatie delen?  Zon schijnt op de rijkste:nieuwe studie onderzoekt hoe zonne-PV voor iedereen haalbaar kan worden
Zon schijnt op de rijkste:nieuwe studie onderzoekt hoe zonne-PV voor iedereen haalbaar kan worden Wat is hydroxoniumzuur?
Wat is hydroxoniumzuur?  Wie heeft natuurkunde geïntroduceerd?
Wie heeft natuurkunde geïntroduceerd?  Hoeveel sterrenstelsels zijn er in Draco Constellation?
Hoeveel sterrenstelsels zijn er in Draco Constellation?  Hoe ontstaat oxidatie bij bananen?
Hoe ontstaat oxidatie bij bananen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

