
Wetenschap
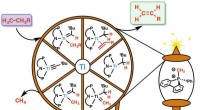
Inzicht in de moleculaire polariteit van HCl:elektronegativiteit en bindingen
Hier is een overzicht:
* Elektronegativiteit: Elektronegativiteit is een maatstaf voor het vermogen van een atoom om elektronen aan te trekken in een chemische binding. Chloor heeft een hogere elektronegativiteit dan waterstof.
* Polaire covalente binding: Wanneer twee atomen met verschillende elektronegativiteiten een binding vormen, worden de gedeelde elektronen sterker naar het meer elektronegatieve atoom getrokken. Hierdoor ontstaat een gedeeltelijke negatieve lading (δ-) op het meer elektronegatieve atoom en een gedeeltelijke positieve lading (δ+) op het minder elektronegatieve atoom.
* HCl-molecuul: In het HCl-molecuul brengen de gedeelde elektronen meer tijd dichter bij het chlooratoom door (vanwege de hogere elektronegativiteit ervan). Hierdoor ontstaat een gedeeltelijk negatieve lading (δ-) op het chlooratoom en een gedeeltelijk positieve lading (δ+) op het waterstofatoom. Deze ongelijkmatige ladingsverdeling resulteert in een polaire covalente binding .
Daarom heeft het HCl-molecuul een dipoolmoment , wat betekent dat het een positief en een negatief uiteinde heeft, waardoor het een polair molecuul is .
 Hoe Negatieve Celsius naar Fahrenheit te converteren
Hoe Negatieve Celsius naar Fahrenheit te converteren  Welk deel van de verbindingen kopercarbonaat CuCo3 is een covalent gebonden polyatomisch ion?
Welk deel van de verbindingen kopercarbonaat CuCo3 is een covalent gebonden polyatomisch ion?  Welke massa NH3 heb je bereid uit de reactie van 10 g N2 met een overmaat aan H2?
Welke massa NH3 heb je bereid uit de reactie van 10 g N2 met een overmaat aan H2?  Wat is de geleidbaarheid van zeewater?
Wat is de geleidbaarheid van zeewater?  Spectroscopische techniek waarbij watermoleculen die op het oppervlak liggen worden opgespoord, laat zien hoe ze ontspannen nadat ze zijn opgewonden
Spectroscopische techniek waarbij watermoleculen die op het oppervlak liggen worden opgespoord, laat zien hoe ze ontspannen nadat ze zijn opgewonden
Hoofdlijnen
- Wat zijn voorbeelden van hoe organismen mitose zijn voor groei en reparatie?
- Hoe dragen mensen bij aan zaadverspreiding?
- De vier eigenschappen van spiercellen
- Uitzonderlijk goed bewaard gebleven gefossiliseerd wormembryo uit de Cambrische periode geïdentificeerd in China
- Welk weefsel van een plant slaat suiker en zetmeel op?
- Hoe genoctrooien werken
- Hoe verschillen eiwitoïde microsferen van cellen?
- Studie ontdekt hoe een systeem van eiwitten Salmonella helpt overleven in macrofagen
- Wat is de organel van de cellen die materialen zoals waterzout -eiwitten en koolhydraten opslaan?
- Slimme materialen die in ultrageluid worden gebruikt, gedragen zich vergelijkbaar met water, chemici melden

- Goedkoop, energiezuinige en schone reactie om chemische grondstof te maken
- Instrument bij BESSY II laat zien hoe licht molybdeendisulfidelagen activeert om katalysatoren te worden

- Niet-giftige technologie haalt meer goud uit erts

- Kleinschalige engineering kan grote vooruitgang brengen in de medische zorg
 welke van deze items trilt omdat er een lichtgolf is gevormd?
welke van deze items trilt omdat er een lichtgolf is gevormd?  Wat zijn de gecontroleerde variabelen van de viscositeit in een vloeistof?
Wat zijn de gecontroleerde variabelen van de viscositeit in een vloeistof?  Wat kenmerkt Precambrian Rock nauwkeurig?
Wat kenmerkt Precambrian Rock nauwkeurig?  Hoe wordt het ene geslacht groter dan het andere?
Hoe wordt het ene geslacht groter dan het andere?  Klimaatverandering brengt nieuw risico met zich mee:zijn binnenvaartbruggen te laag?
Klimaatverandering brengt nieuw risico met zich mee:zijn binnenvaartbruggen te laag? Waar wordt eletromagnetische energie voor gebruikt?
Waar wordt eletromagnetische energie voor gebruikt?  Slimme stoffen mogelijk gemaakt door nieuwe metaaldepositietechniek
Slimme stoffen mogelijk gemaakt door nieuwe metaaldepositietechniek Wat zijn de intermoleculaire krachten tussen c3h7oh?
Wat zijn de intermoleculaire krachten tussen c3h7oh?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

