
Wetenschap
Kw =Ka x Kb:Afleiding voor zuur-base-conjugaatparen in water
1. De evenwichtsreacties:
* Zuurdissociatie: Beschouw een zwak zuur, HA, dat dissocieert in water:
HA(aq) + H₂O(l) ⇌ H₃O⁺(aq) + A⁻(aq)
met een zure dissociatieconstante, Ka:
Ka =[H₃O⁺][A⁻] / [HA]
* Basishydrolyse: De geconjugeerde base, A⁻, ondergaat hydrolyse:
A⁻(aq) + H₂O(l) ⇌ HA(aq) + OH⁻(aq)
met een basehydrolyseconstante, Kb:
Kb =[HA][OH⁻] / [A⁻]
2. De evenwichten combineren:
* De uitdrukkingen Ka en Kb vermenigvuldigen:
Ka * Kb =([H₃O⁺][A⁻] / [HA]) * ([HA][OH⁻] / [A⁻])
* Vereenvoudiging: Merk op dat [HA] en [A⁻] elkaar opheffen.
Ka * Kb =[H₃O⁺][OH⁻]
3. Het ionenproduct van water:
* Kw-definitie: Het ionenproduct van water, Kw, wordt gedefinieerd als:
Kw =[H₃O⁺][OH⁻]
4. De conclusie:
* De vergelijkingen combineren: Omdat we hebben aangetoond dat Ka * Kb =[H₃O⁺][OH⁻] en Kw =[H₃O⁺][OH⁻], kunnen we concluderen:
Kw =Ka * Kb
Daarom is het ionenproduct van water (Kw) gelijk aan het product van de zuurdissociatieconstante (Ka) en de basehydrolyseconstante (Kb) voor een geconjugeerd zuur-basepaar.
Belangrijke opmerking: Deze relatie benadrukt de onderlinge afhankelijkheid van zuur- en basesterkten binnen een geconjugeerd paar. Als één lid van het paar een sterk zuur is (grote Ka), zal de geconjugeerde base een zwakke base zijn (kleine Kb) en omgekeerd. Dit zorgt ervoor dat Kw constant blijft bij een bepaalde temperatuur.
 4 redenen waarom een door gas geleid economisch herstel verschrikkelijk is, naïef idee
4 redenen waarom een door gas geleid economisch herstel verschrikkelijk is, naïef idee Welk klimaat wordt gekenmerkt door matige neerslag en bomen met naaldblad?
Welk klimaat wordt gekenmerkt door matige neerslag en bomen met naaldblad?  Duurzaam toerisme of een selfie? Liefhebbers van ecotoerisme zijn er misschien voor de gram
Duurzaam toerisme of een selfie? Liefhebbers van ecotoerisme zijn er misschien voor de gram Graupel is geen sneeuw, noch natte sneeuw, geen hagel, dus wat is het in vredesnaam?
Graupel is geen sneeuw, noch natte sneeuw, geen hagel, dus wat is het in vredesnaam?  Waarom het economisch gezien niet zinvol is om de klimaatverandering te negeren bij ons herstel van de pandemie
Waarom het economisch gezien niet zinvol is om de klimaatverandering te negeren bij ons herstel van de pandemie
Hoofdlijnen
- Wat is kurkcel?
- Wat betekenen het woord delen in biogeochemische cyclus?
- Wanneer en waarom DNA condenseert tijdens de celcyclus
- Beschrijf de morfologische kenmerken van Amoeba Proteus?
- Bloed is gemaakt van ongeveer één halve cellen en celonderdelen vloeistof genaamd wat?
- Wat heeft Kingdom Fungi dat de ander heeft?
- Lang geleden kruisten mensen en Neanderthalers elkaar:wat gebeurde er met de genen van de Neanderthalers?
- Bijenkoningin of werkbij? Nieuwe inzichten in het beroemde kastenstelsel van de honingbijengemeenschap
- Waar zijn koolhydraten in cellen?
- Onderzoeksteam toont complexe, 3D-geprinte schwarzieten zijn bestand tegen druk wanneer ze zijn gecoat

- Assemblagetheorie zou goed nieuws kunnen zijn voor de ontdekking van medicijnen
- Hoe elektronen worden verdeeld binnen de schillen van een atoom

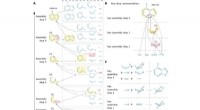
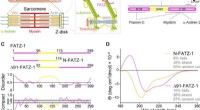
- Orde van wanorde in de sarcomeer
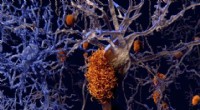
- Ontdekking van hoe amyloïden metaalionen binden werpt licht op de eiwitfunctie
 Hoe schakelen gewas-veeteeltsystemen over op groene landbouwontwikkeling in het Baiyangdian Basin?
Hoe schakelen gewas-veeteeltsystemen over op groene landbouwontwikkeling in het Baiyangdian Basin?  Sneeuw valt anders op nanoschaal
Sneeuw valt anders op nanoschaal Wat is de functie van operatorlocus a lac operon a. Binding met RNA -polymerase b. Het identificeren van substraat lactose c. Messenger produceren d. Codering voor onderdrukker e. Wit?
Wat is de functie van operatorlocus a lac operon a. Binding met RNA -polymerase b. Het identificeren van substraat lactose c. Messenger produceren d. Codering voor onderdrukker e. Wit?  Klimaatbestendige infrastructuur
Klimaatbestendige infrastructuur Wereldwijde waarnemingen bevestigen een exoplaneet met lens in de buurt
Wereldwijde waarnemingen bevestigen een exoplaneet met lens in de buurt Nieuwe technologie en app kunnen bedreigde primaten helpen, langzame illegale handel
Nieuwe technologie en app kunnen bedreigde primaten helpen, langzame illegale handel Superrekbaar, supercompressibele supercondensatoren
Superrekbaar, supercompressibele supercondensatoren Waarom is de zon hernieuwbaar maar niet -hernieuwbaar olie?
Waarom is de zon hernieuwbaar maar niet -hernieuwbaar olie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

