
Wetenschap
Elektrolyse van natriumchloride:waterstof- en natriumverzameling begrijpen
Basisprincipes van elektrolyse
* Elektrolyse: Het proces waarbij elektrische stroom wordt gebruikt om een niet-spontane chemische reactie op gang te brengen.
* Kathode: De negatief geladen elektrode waar reductie (versterking van elektronen) optreedt.
* Anode: De positief geladen elektrode waar oxidatie (verlies van elektronen) optreedt.
De reacties
Tijdens de elektrolyse van NaCl treden de volgende reacties op:
* Bij de kathode (reductie):
* 2H₂O(l) + 2e⁻ → H₂(g) + 2OH⁻(aq) Dit is de reductie van water tot waterstofgas.
* Aan de anode (oxidatie):
* 2Cl⁻(aq) → Cl₂(g) + 2e⁻ Dit is de oxidatie van chloride-ionen om chloorgas te vormen.
Waarom waterstof, en niet natrium?
1. Elektrochemische reeks: De elektrochemische reeks (of activiteitsreeks) vermeldt metalen in volgorde van hun reactiviteit. Natrium is een zeer reactief metaal, wat betekent dat het gemakkelijk elektronen verliest. Waterstof is minder reactief.
* Het is waarschijnlijker dat natrium wordt geoxideerd (elektronen verliest) aan de anode, NIET aan de kathode.
* Het is waarschijnlijker dat waterstof wordt gereduceerd (elektronen winnen) aan de kathode.
2. Overpotentieel: De overpotentiaal is de extra spanning die nodig is om de energiebarrière te overwinnen om een reactie te laten plaatsvinden. Het overpotentiaal voor de reductie van natriumionen is aanzienlijk hoger dan dat voor de reductie van water. Dit maakt de reductie van water tot waterstof het gunstiger proces aan de kathode.
Samenvatting
* Elektrochemische reactiviteit: Waterstof is minder reactief dan natrium, waardoor het waarschijnlijker is dat het aan de kathode wordt gereduceerd.
* Overpotentieel: Het overpotentieel voor waterstofreductie is lager, waardoor de vorming ervan wordt bevorderd ten opzichte van natrium.
Opmerking: Als u een kwikkathode zou gebruiken, zou de overpotentiaal voor natriumreductie worden verlaagd en zou er natriummetaal geproduceerd kunnen worden aan de kathode. Dit is echter een zeer gevaarlijk proces.
 Sterven voor de groep:wat motiveert ultieme opoffering?
Sterven voor de groep:wat motiveert ultieme opoffering?  De enorme branden en giftige nevel in Indonesië zullen de komende jaren gezondheidsproblemen veroorzaken
De enorme branden en giftige nevel in Indonesië zullen de komende jaren gezondheidsproblemen veroorzaken Waarom we een betere filosofie van bomen nodig hebben
Waarom we een betere filosofie van bomen nodig hebben Studies tonen de kwetsbaarheid van Antarctische ecosystemen aan
Studies tonen de kwetsbaarheid van Antarctische ecosystemen aan Door klimaatverandering kunnen koralen het alleen doen
Door klimaatverandering kunnen koralen het alleen doen
Hoofdlijnen
- Orgelsystemen kunnen uit cellen of weefsels worden samengesteld, maar niet beide?
- Welke organel zet glucose om in glycogeen?
- Welk idee van gebaseerd op fossielen en de moderne organismen die hij in feite heeft gevonden, zegt in feite dat genetische veranderingen door latere generaties worden geërfd?
- Wat zijn voorbeelden van traditionele biotechnologie?
- De talen van de wereld kunnen zo op elkaar lijken vanwege de manier waarop mensen over taal praten
- Welk type menselijke cellen bevatten lysosomen?
- Het idee dat alle levende wezens bestaande uit cellen voortkomen uit reeds bestaande worden genoemd?
- Welke organismen fungeren als een brug tussen de stikstof in atmosfeer en van biosfeer?
- Enkele cel ziekteverwekker zonder kern?
- Dynamische hydrogel die wordt gebruikt om zachte robotcomponenten en LEGO-achtige bouwstenen te maken
- Reparatie van kuilen milieuvriendelijk gemaakt met gruis van afvalwaterzuivering

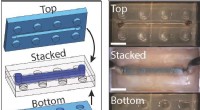
- Niet alle gelaagde structuren van de natuur zijn zo taai als schelpen en geweien van dieren, studie vondsten

- Dubbel gedoteerde koolstofmicrosferen met sterk stikstof en zwavel voor supercondensatoren
- Wetenschappers ontwikkelen een innovatieve methode voor het vullen en afdichten van pleuraholtes

 Het einde is nabij voor Apples iTunes, aangezien de techgigant zich richt op aparte audio- en videomarkten
Het einde is nabij voor Apples iTunes, aangezien de techgigant zich richt op aparte audio- en videomarkten Wetenschapsprojecten over welke appels de meeste Seeds
Wetenschapsprojecten over welke appels de meeste Seeds Pandemie leidt tot infodemie in wetenschappelijke literatuur
Pandemie leidt tot infodemie in wetenschappelijke literatuur In het laboratorium gemaakte zeshoekige diamanten stijver dan natuurlijke diamanten
In het laboratorium gemaakte zeshoekige diamanten stijver dan natuurlijke diamanten Niet-gechloreerde, met oplosmiddel verwerkte hoogwaardige ambipolaire transistors
Niet-gechloreerde, met oplosmiddel verwerkte hoogwaardige ambipolaire transistors Wat is de gemiddelde temperatuur in Irak juli?
Wat is de gemiddelde temperatuur in Irak juli?  Wat verklaring geldt voor zowel mitose als meiose?
Wat verklaring geldt voor zowel mitose als meiose?  Een huis kopen:7 tips om professioneel te onderhandelen
Een huis kopen:7 tips om professioneel te onderhandelen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

