
Wetenschap
Inzicht in activeringsenergie bij chemische reacties
Dit is waarom:
* Activeringsenergie is de minimale hoeveelheid energie die reagerende moleculen moeten bezitten om een reactie op gang te brengen.
* Sommige reacties vereisen veel energie om op gang te komen (zoals het verbranden van hout), terwijl andere gemakkelijk bij kamertemperatuur plaatsvinden (zoals roesten).
* Hoe hoger de activeringsenergie, hoe moeilijker het is om de reactie te laten plaatsvinden.
Factoren die de activeringsenergie beïnvloeden:
* Aard van de reactanten: Sommige moleculen zijn reactiever dan andere.
* Aanwezigheid van een katalysator: Katalysatoren versnellen reacties door de activeringsenergie te verlagen.
* Temperatuur: Hogere temperaturen verhogen de kinetische energie van moleculen, waardoor het voor hen gemakkelijker wordt om de activeringsenergiebarrière te overwinnen.
Laat het me weten als je dit verder wilt onderzoeken!
 Ionische verbindingen begrijpen:vorming, structuur en eigenschappen
Ionische verbindingen begrijpen:vorming, structuur en eigenschappen  Waarom worden verbrandingsreacties beschouwd als uitzonderingen op de regels van chemische reacties?
Waarom worden verbrandingsreacties beschouwd als uitzonderingen op de regels van chemische reacties?  Is suiker uit maïs zuur of basisch op de pH-schaal?
Is suiker uit maïs zuur of basisch op de pH-schaal?  Nieuwe inzichten in fermentatie-enzymen zullen de ecologische voetafdruk van de chemische industrie verkleinen
Nieuwe inzichten in fermentatie-enzymen zullen de ecologische voetafdruk van de chemische industrie verkleinen Hoe scheidt u stoffen in een mengsel?
Hoe scheidt u stoffen in een mengsel?
 Zomerdroogte kan de aanvoer van Franse puds doen slinken
Zomerdroogte kan de aanvoer van Franse puds doen slinken Er is een gigantische scheur in een Antarctische ijsplaat. Moeten we ons zorgen maken?
Er is een gigantische scheur in een Antarctische ijsplaat. Moeten we ons zorgen maken? NASA-satellietbeelden tonen evolutie van orkaan Harvey
NASA-satellietbeelden tonen evolutie van orkaan Harvey Rechtbank zegt dat het bevel om olieboringen in Everglades toe te staan ten onrechte is uitgevaardigd
Rechtbank zegt dat het bevel om olieboringen in Everglades toe te staan ten onrechte is uitgevaardigd Een beter begrip van de groei van koraalskeletten suggereert manieren om riffen te herstellen
Een beter begrip van de groei van koraalskeletten suggereert manieren om riffen te herstellen
Hoofdlijnen
- Uit onderzoek blijkt hoe de adelborstvis zijn urenlange paringsroep volhoudt
- Wat is de functie van de eiercel?
- Het maken van RNA op basis van de sequentielucleotiden in DNA wordt genoemd?
- Wat zijn de drie belangrijkste componenten van de kern?
- Gebruiken paddenstoelen echt taal om met elkaar te praten? Een schimmelexpert onderzoekt
- Wat zijn twee soorten eiwitten?
- Wat zijn de algemeen goede eigenschappen van de bioloog?
- Wat is bifocale informatica?
- Schildpad die vislijn heeft ingeslikt, losgelaten in oceaan
- Gevriesdroogde aardbeien en ijs zorgen voor een zeer stabiele relatie

- Slim bulkplastic reageert op licht, temperatuur en vochtigheid

- De verrassende flexibiliteit van kristaloppervlakken vastleggen

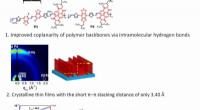
- Organische elektronica:wetenschappers ontwikkelen een hoogwaardige unipolaire n-type dunne-filmtransistor
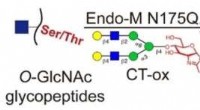
- Reversibele chemo-enzymatische labelstrategie maakt diepgaande analyse van eiwit O-GlcNAcylation mogelijk
 Hoe is Earth Day geëvolueerd?
Hoe is Earth Day geëvolueerd?  Een studie kijkt naar de transformatie van de Europese cinema via Studiocanal
Een studie kijkt naar de transformatie van de Europese cinema via Studiocanal Wanneer elementen chemisch samen binden, maken ze een?
Wanneer elementen chemisch samen binden, maken ze een?  Wat is een vergelijking voor kale boom?
Wat is een vergelijking voor kale boom?  Het ontrafelen van het wanneer, waar en hoe van vulkaanuitbarstingen
Het ontrafelen van het wanneer, waar en hoe van vulkaanuitbarstingen  Partizanenpolarisatie helpt het Congres om rekeningen aan te nemen:studie
Partizanenpolarisatie helpt het Congres om rekeningen aan te nemen:studie Bosch-ingenieurs richten zich op het opfleuren van de toekomst van diesel
Bosch-ingenieurs richten zich op het opfleuren van de toekomst van diesel Hoeveel atomen zijn er in 1 mol Fe?
Hoeveel atomen zijn er in 1 mol Fe?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

