
Wetenschap
Waterstofbinding en de oplosmiddelkracht van water:polariteit begrijpen
Dit is waarom:
* Polaire covalente binding: De binding tussen waterstof en zuurstof is een polaire covalente binding. Dit betekent dat de elektronen in de binding niet gelijkelijk verdeeld zijn tussen de twee atomen. Zuurstof is elektronegatiever dan waterstof, wat betekent dat het de gedeelde elektronen sterker aantrekt. Hierdoor ontstaat een gedeeltelijke negatieve lading op het zuurstofatoom (δ-) en een gedeeltelijke positieve lading op de waterstofatomen (δ+).
* Water als dipool: Deze ongelijkmatige verdeling van de lading maakt het watermolecuul tot een dipool, met een positief uiteinde en een negatief uiteinde.
* Aantrekking tot ionen en polaire moleculen: Het positieve uiteinde van een watermolecuul wordt aangetrokken door het negatieve uiteinde van andere polaire moleculen of ionen. Het negatieve uiteinde van een watermolecuul wordt aangetrokken door het positieve uiteinde van andere polaire moleculen of ionen. Door deze aantrekkingskracht kan water veel verschillende stoffen omringen en oplossen.
Samengevat: De polaire aard van de waterstof-zuurstofbinding in watermoleculen creëert een dipoolmoment, waardoor water via elektrostatische interacties sterk kan interageren met andere polaire moleculen en ionen. Deze sterke interactie is de belangrijkste reden waarom water een uitstekend oplosmiddel is.
 Waar of onwaar behoud in de wetenschap verwijst naar de hoeveelheid hoeveelheid die voor en na een evenement hetzelfde blijft?
Waar of onwaar behoud in de wetenschap verwijst naar de hoeveelheid hoeveelheid die voor en na een evenement hetzelfde blijft?  Risico's van natuurbranden verminderen voor beter beheer en een betere toewijzing van middelen
Risico's van natuurbranden verminderen voor beter beheer en een betere toewijzing van middelen De nieuwe wet waarbij Puget Sound Energy betrokken is, streeft ernaar een koers voor de toekomst uit te zetten
De nieuwe wet waarbij Puget Sound Energy betrokken is, streeft ernaar een koers voor de toekomst uit te zetten  Hoe beïnvloedt een niet-native plant een ecosysteem?
Hoe beïnvloedt een niet-native plant een ecosysteem?  Opeenvolging van vegetatie beïnvloedt de bodemkwaliteit in het subtropische karstlandschap van China
Opeenvolging van vegetatie beïnvloedt de bodemkwaliteit in het subtropische karstlandschap van China
Hoofdlijnen
- Wat is transcriptie en wat zijn de belangrijkste stappen in dit proces?
- Hoe veroorzaakt allel een eigenschap in een organisme?
- Wat is een structuur of gedrag dat de kans op het overleven van soorten vergroot?
- Wat zijn halfgeleiders?
- Welk deel van de stamcellen biedt instructies om het hart te bouwen?
- Tropische bodems zeer gevoelig voor opwarming van de aarde, waarschuwen onderzoekers
- Wat wordt gevormd in rood beenmerg en zijn het meest voorkomende type witte bloedcellen?
- Hoe heet een graad in de mariene biologie?
- Welke verantwoordelijkheden hebben wetenschappers en waarom?
- Chemputer belooft app-gestuurde revolutie voor medicijnproductie

- Foto-responsieve eiwithydrogels als middel voor gecontroleerde afgifte van stamcellen/eiwitten
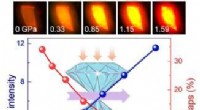
- Druk onderdrukt het opsluiten van dragers in 2-D halide perovskiet
- Nanosensoren verbeteren de detectie van biomarkers voor ziekten in uitgeademde adem
- Op maat gemaakte enzymatische oplossingen verminderen de tijd en kosten van bioraffinageprocessen

 Verschillen tussen kikkersoorten laten zien hoe ontwikkelingspatronen verband houden met diversiteit
Verschillen tussen kikkersoorten laten zien hoe ontwikkelingspatronen verband houden met diversiteit  Hoe beïnvloedt de zwaartekracht de derde bewegingswet?
Hoe beïnvloedt de zwaartekracht de derde bewegingswet?  Controle vergroten:de vorm van de propeller helpt nanodeeltjes te sturen, zeggen onderzoekers
Controle vergroten:de vorm van de propeller helpt nanodeeltjes te sturen, zeggen onderzoekers  Wat wordt macromolecuul gevormd als monomeren samenvoegen?
Wat wordt macromolecuul gevormd als monomeren samenvoegen?  Wat is een optisch apparaat dat vaak wordt gebruikt om wit licht te breken?
Wat is een optisch apparaat dat vaak wordt gebruikt om wit licht te breken?  Waarom moet een niet -digitale klok mechanisch omzetten van elektrische energie?
Waarom moet een niet -digitale klok mechanisch omzetten van elektrische energie?  Methaan heeft vier covalente bindingen en hoeveel eenzame paren?
Methaan heeft vier covalente bindingen en hoeveel eenzame paren?  Waarom is zuurstof slecht in fruit?
Waarom is zuurstof slecht in fruit?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

