
Wetenschap
pH-veranderingen tijdens zure verdunning:het proces begrijpen
* pH en zuurgraad: pH is een maatstaf voor de concentratie waterstofionen (H+) in een oplossing. Een lagere pH duidt op een hogere H+-concentratie, waardoor de oplossing zuurder wordt.
* Verdunning: Verdunning houdt in dat meer oplosmiddel (in dit geval water) aan een oplossing wordt toegevoegd. Dit verlaagt de concentratie van de opgeloste stof (zuur) in de oplossing.
* Verlaagde concentratie van H+: Omdat het zuur nu over een groter volume wordt verspreid, neemt de concentratie H+-ionen af.
* pH-verhoging: Naarmate de H+-concentratie afneemt, neemt de pH-waarde toe, richting een meer neutrale waarde (7).
Voorbeeld:
Stel je voor dat je een sterk zuur zoals zoutzuur (HCl) in een geconcentreerde oplossing hebt. Deze oplossing heeft een lage pH (bijvoorbeeld 1). Als je deze oplossing verdunt met water, neemt de concentratie HCl af en dus ook de concentratie H+-ionen. Dit resulteert in een hogere pH (bijvoorbeeld 3).
Belangrijke opmerking: Hoewel verdunning over het algemeen de pH verhoogt, is het belangrijk om te onthouden dat sterke zuren zelfs na verdunning sterke zuren blijven. Ze zullen nog steeds een aanzienlijk aantal H+-ionen bevatten, zelfs als de pH hoger is.
 Levende elektroden met bacteriën en organische elektronica
Levende elektroden met bacteriën en organische elektronica Wat is Magnesiumcarbonaat?
Wat is Magnesiumcarbonaat?
Magnesiumcarbonaat is een geurloos wit poeder met verschillende industriële toepassingen. Het komt voor in de natuur of als een gefabriceerde stof.
Identificatie
De chemische formule voor magnesiumcarbon
 Welke nuttige stof maakt fotosynthese voor de plant?
Welke nuttige stof maakt fotosynthese voor de plant?  De stikstofbasis aan welke guaninebindingen?
De stikstofbasis aan welke guaninebindingen?  Welk proces vertegenwoordigt een chemische verandering ... smelten van ijs of verdampingswater?
Welk proces vertegenwoordigt een chemische verandering ... smelten van ijs of verdampingswater?
 Wereld moet tegen 2020 actie ondernemen om op hol geslagen klimaatverandering te voorkomen:VN-chef
Wereld moet tegen 2020 actie ondernemen om op hol geslagen klimaatverandering te voorkomen:VN-chef Onderzoek toont aan dat water honderden meters onder het oppervlak van Lake Michigan aan het opwarmen is
Onderzoek toont aan dat water honderden meters onder het oppervlak van Lake Michigan aan het opwarmen is Fracking laat een zware voetafdruk achter in Patagonië in Argentinië
Fracking laat een zware voetafdruk achter in Patagonië in Argentinië Vernietigt de opwarming van de aarde de Mount Everest?
Vernietigt de opwarming van de aarde de Mount Everest?  Wat is een voorbeeld van principe?
Wat is een voorbeeld van principe?
Hoofdlijnen
- Welke klier heeft meer exocrien dan endocrien weefsel?
- Is een hond een organische vorm?
- Wat doen ATP -synthasemoleculen?
- Wat betekent scierose?
- Welk proces moet de cel gebruiken om eiwit binnen te laten en waarom?
- Wat voor soort cellen ontwikkelen zich uit stamcellen van Uni-potte?
- Waarom zijn Archaea in een ander domein dan bacteriën?
- Waarom worden enkele celorganismen zoals bacteriën groeien om de grootte van een kleine vis te worden?
- Zijn dierenmigraties sociaal?
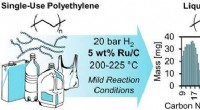
- Een milde manier om plastic in flessen te upcyclen tot brandstof en andere hoogwaardige producten
- MOF-gebaseerde sensor voor het testen van de waterkwaliteit

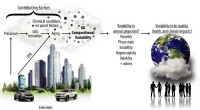
- Wat hangt er in de lucht? Er komt meer bij kijken dan we dachten
- Dit servies van suikerriet en bamboe breekt in 60 dagen af

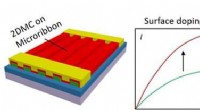
- 2-D moleculaire kristallen die de elektronische eigenschappen van organische halfgeleiders moduleren
 Een van de acht basissrotsvormende mineralen?
Een van de acht basissrotsvormende mineralen?  Watertankers blijken een reddingslijn voor uitgedroogde dorpen in India
Watertankers blijken een reddingslijn voor uitgedroogde dorpen in India Waar wordt biotiet mica gedolven?
Waar wordt biotiet mica gedolven?  Hoe kan stamcelonderzoek de gemeenschap beïnvloeden?
Hoe kan stamcelonderzoek de gemeenschap beïnvloeden?  Welke afstand tot de aarde werd eerst gemeten?
Welke afstand tot de aarde werd eerst gemeten?  Wat is tangentiële snelheid en versnelling?
Wat is tangentiële snelheid en versnelling?  Kunnen de deeltjes die een vaste bewegen bestaan langzamer of sneller dan gas?
Kunnen de deeltjes die een vaste bewegen bestaan langzamer of sneller dan gas?  Wat zijn de energiebronnen die u elke dag gebruikt?
Wat zijn de energiebronnen die u elke dag gebruikt?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

