
Wetenschap
De moleculaire geometrie van NBr3 begrijpen:een stapsgewijze handleiding
* Lewis-structuur: Stikstof (N) is het centrale atoom waaraan drie broomatomen (Br) zijn gebonden. Stikstof heeft ook één eenzaam elektronenpaar.
* Elektronengeometrie: De elektronengeometrie is tetraëdrisch omdat er vier elektronendomeinen rond het centrale stikstofatoom zijn (drie bindingsparen en één alleenstaand paar).
* Moleculaire geometrie: Het eenzame paar op stikstof stoot de bindingsparen af, waardoor de broomatomen dichter bij elkaar worden gedrukt. Dit resulteert in een trigonale piramide vorm.
Visuele weergave:
Stel je een piramide voor met bovenaan een stikstofatoom en onderaan de drie broomatomen. Het eenzame paar op stikstof wijst weg van de basis van de piramide.
 Gaan atomen met één op het periodiek systeem in eiwitten en neutronen?
Gaan atomen met één op het periodiek systeem in eiwitten en neutronen?  Is chroom (III) nitraat oplosbaar in water?
Is chroom (III) nitraat oplosbaar in water?  Het Miller-Urey-experiment:waarom deze gassen zijn gekozen
Het Miller-Urey-experiment:waarom deze gassen zijn gekozen  Wat ioniseert volledig in oplossing en wordt als een sterk zuur beschouwd?
Wat ioniseert volledig in oplossing en wordt als een sterk zuur beschouwd?  Op pijnboomsap gebaseerd plastic:een potentiële gamechanger voor de toekomst van duurzame materialen
Op pijnboomsap gebaseerd plastic:een potentiële gamechanger voor de toekomst van duurzame materialen
 NASA kijkt naar regenvalintensiteit in tropische depressie Bolaven
NASA kijkt naar regenvalintensiteit in tropische depressie Bolaven Deeltjes die worden uitgestoten door 3D-printers voor consumenten kunnen de luchtkwaliteit binnenshuis schaden
Deeltjes die worden uitgestoten door 3D-printers voor consumenten kunnen de luchtkwaliteit binnenshuis schaden Hoe planten omgaan met calcium kan de effecten van zure regen verminderen
Hoe planten omgaan met calcium kan de effecten van zure regen verminderen  Soorten krabben op de New Jersey Shore
Soorten krabben op de New Jersey Shore Het klimaat ontvluchten:de grote migratie die voor ons ligt
Het klimaat ontvluchten:de grote migratie die voor ons ligt
Hoofdlijnen
- Het gebruik van DNA -informatie om de productie te sturen die bepaalde eiwitten worden gericht, wordt aangeroepen?
- Maki's darmmicrobioom sterk beïnvloed door sociale kringen, studie zegt:
- Is een boombiologische vector?
- Wat betekent een cel?
- Wetenschap kan beantwoorden wat voor soort vragen?
- Hoe worden nieuwe weefsels en organen gedurende het leven van een plant geproduceerd?
- Hoe overvloedig zijn eencellige en meercellige organismen?
- Wat betekent consumenten in de biologie?
- Gen-experts gaan ongediertebestrijding aanpakken
- RNA-basisbouwsteen voor het eerst biokatalytisch geproduceerd
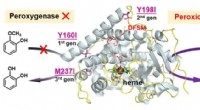
- P450-peroxygenase omzetten in peroxidase via mechanismegestuurde eiwittechnologie
- Lab doorbraak in 3D printen van glas

- Mechanische kracht regelt de snelheid van eiwitsynthese
- Termietendarmmicroben kunnen de productie van biobrandstoffen ondersteunen

 Een project van Russische wetenschappers zal helpen bij het maken van capsules voor gerichte medicijnafgifte
Een project van Russische wetenschappers zal helpen bij het maken van capsules voor gerichte medicijnafgifte Dit gebeurt er met onze plasticrecycling als het offshore gaat
Dit gebeurt er met onze plasticrecycling als het offshore gaat Moleculair jodium katalyseert processen voor antivirale en farmaceutische syntheses
Moleculair jodium katalyseert processen voor antivirale en farmaceutische syntheses Ford gaat over-the-air software-updates aanbieden in de hele line-up
Ford gaat over-the-air software-updates aanbieden in de hele line-up Is generalisatie belangrijk voor laboratoriumapparatuur?
Is generalisatie belangrijk voor laboratoriumapparatuur?  Catastrofale gevolgen voor oceanen wanneer klimaatverandering en crises door plasticvervuiling samengaan
Catastrofale gevolgen voor oceanen wanneer klimaatverandering en crises door plasticvervuiling samengaan Elektronen in sommige keramische kristallen lijken op een bekende manier te verdwijnen
Elektronen in sommige keramische kristallen lijken op een bekende manier te verdwijnen Een jetliner van 747 kruist met een snelheid van 520 mijl per uur. Wat het uur in kilometers?
Een jetliner van 747 kruist met een snelheid van 520 mijl per uur. Wat het uur in kilometers?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

