
Wetenschap
Moleculaire vorm en eigenschappen:een uitgebreide gids
Fysieke eigenschappen:
* Smelt- en kookpunten: Lineaire moleculen met zwakke intermoleculaire krachten hebben doorgaans lagere smelt- en kookpunten in vergelijking met complexere, vertakte moleculen met sterkere krachten.
* Dichtheid: De pakkingsefficiëntie van moleculen in vaste of vloeibare toestand wordt beïnvloed door de vorm.
* Oplosbaarheid: De vorm van een molecuul bepaalt hoe goed het kan interageren met oplosmiddelmoleculen.
* Dampdruk: De vorm van een molecuul kan van invloed zijn op hoe gemakkelijk het verdampt, wat verband houdt met de dampdruk.
Chemische eigenschappen:
* Reactiviteit: De vorm van een molecuul bepaalt welke delen van het molecuul worden blootgesteld en dus beschikbaar zijn voor reactie. Een molecuul met daarin een specifieke functionele groep zal bijvoorbeeld minder reactief zijn vergeleken met een molecuul waarin de functionele groep is blootgesteld.
* Reactiemechanisme: De vorm van een molecuul kan het verloop van een chemische reactie beïnvloeden.
* Stereochemie: De vorm van een molecuul kan leiden tot verschillende stereo-isomeren, dit zijn moleculen met dezelfde atomen maar verschillende ruimtelijke arrangementen. Stereo-isomeren kunnen verschillende biologische activiteiten hebben.
Biologische eigenschappen:
* Enzymactiviteit: Enzymen zijn eiwitten met specifieke vormen waardoor ze kunnen binden aan specifieke moleculen die substraten worden genoemd. De vorm van het substraat is van cruciaal belang voor de enzym-substraatinteractie en dus voor de enzymactiviteit.
* Drugsactie: De vorm van een medicijnmolecuul bepaalt hoe goed het zich kan binden aan de doelreceptor, wat de effectiviteit en mogelijke bijwerkingen beïnvloedt.
* Biologische herkenning: Cellen en organismen herkennen elkaar via moleculen op hun oppervlak. De vormen van deze moleculen zijn cruciaal voor deze herkenningsgebeurtenissen.
Andere verschijnselen:
* Kristalstructuur: De vorm van een molecuul beïnvloedt hoe het zich in een kristalrooster samenpakt.
* Optische eigenschappen: De vorm van een molecuul kan de interactie met licht beïnvloeden, wat kan leiden tot verschijnselen als dubbele breking.
Voorbeelden:
* Water: Door de gebogen vorm van water kan het waterstofbruggen vormen, waardoor het unieke eigenschappen krijgt, zoals een hoog kookpunt en een uitstekend oplosmiddelvermogen.
* DNA: De dubbele helixvorm van DNA zorgt voor efficiënte opslag en replicatie van genetische informatie.
* Eiwitten: De ingewikkelde vormen van eiwitten bepalen hun functies, variërend van het transporteren van zuurstof in het bloed (hemoglobine) tot het katalyseren van chemische reacties (enzymen).
Samengevat: De vorm van een molecuul is een kritische factor die het gedrag en de interacties ervan beïnvloedt, en speelt een belangrijke rol in een groot aantal chemische, biologische en fysische verschijnselen.
 Waterstof en zuurstof:elementen, geen faseveranderingen - een eenvoudige uitleg
Waterstof en zuurstof:elementen, geen faseveranderingen - een eenvoudige uitleg  Onderzoekers fabriceren bio-vriendelijke röntgendetectoren op basis van metaalvrije perovskiet-eenkristallen
Onderzoekers fabriceren bio-vriendelijke röntgendetectoren op basis van metaalvrije perovskiet-eenkristallen Esdoornbladextract kan huidrimpels in de kiem smoren
Esdoornbladextract kan huidrimpels in de kiem smoren Leg uit waarom de gloeidraad van metaal moet worden gemaakt?
Leg uit waarom de gloeidraad van metaal moet worden gemaakt?  Kunnen anionen worden geclassificeerd als zuur of basisch?
Kunnen anionen worden geclassificeerd als zuur of basisch?
Hoofdlijnen
- Is het waar dat wanneer sommige leden van een soort geïsoleerd raken, ze minder snel nieuwe soorten vormen?
- Wat zijn veel voorkomende dingen die niet -cellulair zijn?
- Welke uitgangsmaterialen hebben cellen nodig voor cellulaire ademhaling?
- Wat moet er genetisch een nieuwe soort vormen?
- Wat voor invloed zal klimaatverandering hebben op waar hooggelegen alpenvogels leven?
- Genetische analyses laten zien hoe symbiotische bacteriën in de termietendarm in de loop van de evolutie zijn veranderd
- Wat is polygene erfenis?
- Wat is het resultaat van twee genen die zich op hetzelfde chromosoom bevinden, maar ze zijn ver uit elkaar?
- Wat voor soort microscoop kan worden gebruikt om organellen te bestuderen?
- Vergroening van biomaterialen en steigers die worden gebruikt in regeneratieve geneeskunde

- De crunch houden in vetarme chips

- Gezonde organellen, gezonde cellen

- Onderzoekers beoordelen de snelle vooruitgang in machine learning voor de chemische wetenschappen

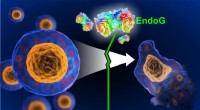
- Biochemici ontdekken een enzym om celdood te stoppen
 In welk halfrond is de constellatie -kanker die wordt gezien?
In welk halfrond is de constellatie -kanker die wordt gezien?  Wat verklaart een enorme diversiteit aan antigenen op welke B -cellen kunnen reageren?
Wat verklaart een enorme diversiteit aan antigenen op welke B -cellen kunnen reageren?  Wat is een voorbeeld van commensalisme in de Alpine?
Wat is een voorbeeld van commensalisme in de Alpine?  Welk van het orgel in je lichaam produceert onmiddellijke energie?
Welk van het orgel in je lichaam produceert onmiddellijke energie?  Zwaartekrachtgegevens van Dawn suggereren dat de koepel op Ceres is gemaakt van vulkanische modder
Zwaartekrachtgegevens van Dawn suggereren dat de koepel op Ceres is gemaakt van vulkanische modder Wat voor soort reactie is MGO H20?
Wat voor soort reactie is MGO H20?  Heeft Moon zijn eigen baan?
Heeft Moon zijn eigen baan?  De functie van de gecodeerde instructies in lichaamscellen is een organisme?
De functie van de gecodeerde instructies in lichaamscellen is een organisme?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

