
Wetenschap
Inzicht in polaire covalente bindingen:ongelijke elektronendeling
Dit is waarom:
* Covalente bindingen houdt het delen van elektronen tussen atomen in.
* Polaire covalente bindingen treedt op wanneer de elektronen ongelijk verdeeld zijn. Dit gebeurt omdat het ene atoom in de binding een sterkere aantrekkingskracht heeft op de gedeelde elektronen dan het andere. Dit atoom is meer elektronegatief.
* Door de ongelijke verdeling ontstaat er een gedeeltelijk positieve lading op het minder elektronegatieve atoom en een gedeeltelijk negatieve lading op het meer elektronegatieve atoom.
Dit verschil in lading creëert een dipoolmoment , wat betekent dat het molecuul een positief en een negatief uiteinde heeft.
Voorbeelden van polaire covalente bindingen zijn onder meer:
* Water (H₂O): Zuurstof is elektronegatiever dan waterstof, dus de elektronen worden dichter bij het zuurstofatoom getrokken, waardoor het zuurstofuiteinde gedeeltelijk negatief wordt en het waterstofuiteinde gedeeltelijk positief.
* Waterstofchloride (HCl): Chloor is elektronegatiever dan waterstof, waardoor de elektronen dichter bij het chlooratoom worden getrokken.
Bedenk dat een polaire covalente binding een soort covalente binding is waarbij de elektronen niet gelijkmatig worden verdeeld. Dit verschil in ladingsverdeling leidt ertoe dat het molecuul een dipoolmoment heeft, wat een cruciale factor is bij het bepalen van de eigenschappen en reactiviteit ervan.
 Wat is het effect van temperatuurverandering tot hoeveelheid warmte -inhoud van de inhoud?
Wat is het effect van temperatuurverandering tot hoeveelheid warmte -inhoud van de inhoud?  Waarom wordt zwavel gebruikt bij vulcanisatie van rubber?
Waarom wordt zwavel gebruikt bij vulcanisatie van rubber?  Chemici gebruiken licht om biologisch actieve verbindingen te bouwen
Chemici gebruiken licht om biologisch actieve verbindingen te bouwen Nieuwe techniek lokaliseert locaties van individuele moleculen in hun cellulaire buurten
Nieuwe techniek lokaliseert locaties van individuele moleculen in hun cellulaire buurten Welk percentage waterstof in peroxide?
Welk percentage waterstof in peroxide?
 Wetenschappers maken 's werelds eerste 3D-warmtebeeld van vulkaan
Wetenschappers maken 's werelds eerste 3D-warmtebeeld van vulkaan Het vangen van diversiteit aan vissoorten betekent een stabieler inkomen voor vissers
Het vangen van diversiteit aan vissoorten betekent een stabieler inkomen voor vissers Wat is de waterconditie van een bladverliezend bos?
Wat is de waterconditie van een bladverliezend bos?  Onderzoek suggereert dat het smelten van Arctische permafrost enorme hoeveelheden lachgas kan vrijgeven
Onderzoek suggereert dat het smelten van Arctische permafrost enorme hoeveelheden lachgas kan vrijgeven Hoe Tree of Life verklaart zowel eenheid als het diversiteitsleven?
Hoe Tree of Life verklaart zowel eenheid als het diversiteitsleven?
Hoofdlijnen
- Complexe levensvormen zijn gedurende lange periodes geëvolueerd door eenvoudiger vormen?
- In welk deel van de cel gebeurt cellulaire ademhaling?
- Wat is Sabacious Bland?
- Waarom het laten ontsnappen van zalm gunstig zou kunnen zijn voor beren en vissers
- Hoe ontwikkelen en groeien Amphebians?
- Hoe reproduceert een huisvlieg zich?
- Wat betekent niet-genetisch?
- Wat doodt de Minnesota-eland? Onderzoekers lanceren nieuwe inspanningen om erachter te komen
- Grootste database over zoogdieren in Portugal nu beschikbaar
- Lab produceert eenvoudige fluorescerende oppervlakteactieve stoffen
- Om de peilstokdiagnose en omgevingstests te verbeteren, voeg gewoon tape toe

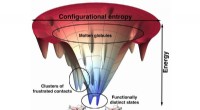
- Atomaire resolutie-eiwitmodellen onthullen nieuwe details over eiwitbinding
- Bewijs van waterdraden gemotiveerd door een biologisch waterkanaal

- Superkritisch antwoord op afgewerkte olie gevonden

 Willekeurige bewegingen helpen kleurdetecterende cellen om het juiste patroon te vormen
Willekeurige bewegingen helpen kleurdetecterende cellen om het juiste patroon te vormen Een object versnelt als zijn blanco of snelheid verandert?
Een object versnelt als zijn blanco of snelheid verandert?  Vorming van natriumionen:elektronenverlies en kationen begrijpen
Vorming van natriumionen:elektronenverlies en kationen begrijpen  In welke dieren bereikt zuurstof alle cellen door het proces van diffusie?
In welke dieren bereikt zuurstof alle cellen door het proces van diffusie?  Simulaties laten zien hoe bèta-amyloïde neurale cellen kan doden
Simulaties laten zien hoe bèta-amyloïde neurale cellen kan doden  Zijn mensen de nieuwe supercomputer? Team vervaagde grenzen tussen man en Mac
Zijn mensen de nieuwe supercomputer? Team vervaagde grenzen tussen man en Mac  Hoeveel meters zijn er in 9,5 voet?
Hoeveel meters zijn er in 9,5 voet?  Hoe scheid je een mengsel van zwavel en houtskool?
Hoe scheid je een mengsel van zwavel en houtskool?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

