
Wetenschap
Molen water geproduceerd uit waterstofgas:een stapsgewijze handleiding
1. Schrijf de uitgebalanceerde chemische vergelijking:
2 H₂ (g) + O₂ (g) → 2 H₂O (l)
Deze vergelijking vertelt ons dat 2 mol waterstofgas (H₂) reageert met 1 mol zuurstofgas (O₂) en 2 mol water (H₂O) produceert.
2. Bepaal de molverhouding:
De uitgebalanceerde vergelijking toont een molverhouding van 2:2 tussen waterstofgas en water. Dit betekent dat voor elke 2 mol waterstofgas er 2 mol water wordt geproduceerd.
3. Bereken het aantal mol water:
Omdat de molverhouding 2:2 is, is het aantal geproduceerde mol water gelijk aan het aantal gebruikte mol waterstofgas:
Mol H₂O =Mol H₂ =1,4 mol
Daarom wordt 1,4 mol water geproduceerd uit de volledige reactie van 1,4 mol waterstofgas.
 Beschrijf één ecosysteem dat in een park kan worden gevonden?
Beschrijf één ecosysteem dat in een park kan worden gevonden?  De Biden-regel verhoogt de vergoedingen voor olieprojecten op openbare gronden
De Biden-regel verhoogt de vergoedingen voor olieprojecten op openbare gronden  Droogte en klimaatverandering verschuiven boomziekte in Sierra Nevada
Droogte en klimaatverandering verschuiven boomziekte in Sierra Nevada Internationale SWOT-satelliet om 's werelds water te onderzoeken
Internationale SWOT-satelliet om 's werelds water te onderzoeken De oorzaken en risico's van de Amazonebranden
De oorzaken en risico's van de Amazonebranden
Hoofdlijnen
- Cellulaire ademhaling:een energievrijgevend proces uitgelegd
- De fasen van het cardiale actiepotentieel begrijpen:een uitgebreide gids
- Wetenschappelijke reproduceerbaarheid:zorgen voor betrouwbaar onderzoek
- Wat is de basiseenheid van het leven? Cellen begrijpen
- Aan het begin van de metafase zijn alle chromosomen?
- De eigenschappen van een organisme worden gecontroleerd door zijn?
- Hoe adaptieve veranderingen in cellulaire vloeistoffen het leven in zee in staat stellen om te gaan met abiotische stressoren
- Welke soorten schimmels?
- Wat betekent hypothese in de wetenschappelijke methode?
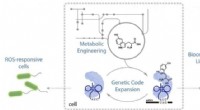
- Chemici breiden genetische code van E. coli uit om 21e aminozuur te produceren, het nieuwe vaardigheden geven
- 3D-geprinte polymeerstents groeien mee met pediatrische patiënten en worden na verloop van tijd biologisch afgebroken

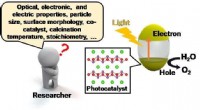
- De reis naar schone energie versnellen door optimalisatie van fotokatalysatoren
- Hoe een reactie in een chemische vergelijking te identificeren

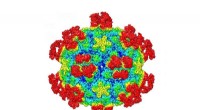
- Nieuw mechanisme om virussen te vernietigen kan leiden tot toekomstige therapieën
 Welke dingen zijn constant in beweging?
Welke dingen zijn constant in beweging?  Magnetische microrobots gebruiken capillaire krachten om deeltjes op hun plaats te krijgen
Magnetische microrobots gebruiken capillaire krachten om deeltjes op hun plaats te krijgen Wazige luchten, slechte luchtkwaliteit:verergert de havencongestie de vervuiling van LA?
Wazige luchten, slechte luchtkwaliteit:verergert de havencongestie de vervuiling van LA? Wat is de chemische naam voor HCO3Na?
Wat is de chemische naam voor HCO3Na?  Wat zijn de meest primitieve organismen die tegenwoordig een structuur hebben die te simpel is als cellen.?
Wat zijn de meest primitieve organismen die tegenwoordig een structuur hebben die te simpel is als cellen.?  Wat gebeurt er met de snelheid van planeten in een baan om de zon terwijl je dichter de zon komt?
Wat gebeurt er met de snelheid van planeten in een baan om de zon terwijl je dichter de zon komt?  Wat voor soort erosie is een klif?
Wat voor soort erosie is een klif?  Hoe zijn de concentraties van hydroniumionen en hydroxide in waterige oplossingen gerelateerd?
Hoe zijn de concentraties van hydroniumionen en hydroxide in waterige oplossingen gerelateerd?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

