
Wetenschap
Fenolftaleïne in zuur-base-titraties:indicatoreigenschappen en -functie
Hier is hoe het werkt:
* Fenolftaleïne is kleurloos in zure oplossingen. Dit komt omdat het molecuul zich in zijn geprotoneerde vorm bevindt, die kleurloos is.
* Fenolftaleïne is roze in basische oplossingen. In basische oplossingen verliest het molecuul een proton en wordt het gedeprotoneerd. De gedeprotoneerde vorm is roze.
Tijdens de titratie voegt u een base (bijvoorbeeld NaOH) toe aan een zure oplossing (bijvoorbeeld HCl). Naarmate de base wordt toegevoegd, neemt de pH van de oplossing geleidelijk toe.
* Op het equivalentiepunt , de mol zuur en base zijn gelijk en de oplossing is neutraal (pH =7).
* Het eindpunt is het punt waarop de indicator van kleur verandert, wat iets voorbij het equivalentiepunt ligt.
Door de kleurverandering van fenolftaleïne zorgvuldig te observeren, kunnen we het eindpunt van de titratie bepalen. Hierdoor kunnen we de onbekende concentratie van de zuur- of base-oplossing berekenen.
Samengevat: Fenolftaleïne is een waardevol hulpmiddel bij zuur-base-titraties omdat het visueel het eindpunt van de reactie aangeeft, waardoor een nauwkeurige bepaling van de onbekende concentratie mogelijk is.
 Welke verbindingen hebben veel algen om hen te helpen licht te absorberen bij verschillende wavelenghts?
Welke verbindingen hebben veel algen om hen te helpen licht te absorberen bij verschillende wavelenghts?  Wat doen moleculen wanneer warmte wordt overgedragen door geleiding?
Wat doen moleculen wanneer warmte wordt overgedragen door geleiding?  Hoe ontdekten wetenschappers pangea?
Hoe ontdekten wetenschappers pangea?  3D-experimenten werpen nieuw licht op legeringen met vormgeheugen
3D-experimenten werpen nieuw licht op legeringen met vormgeheugen Waarom dicteert de wet van behoudsmassa dat chemische vergelijkingen in evenwicht zijn?
Waarom dicteert de wet van behoudsmassa dat chemische vergelijkingen in evenwicht zijn?
Hoofdlijnen
- Welk type cel of structuur is de eerste fase elke seksuele levenscyclus?
- Vogelambassadeurs en tribale perspectieven:een vogelperspectief van voorgeschreven vuur
- Officiële vishandel onderschat wereldwijde vangsten enorm
- Hoe worden glucosemoleculen in de cel verplaatst en welk transport is dit?
- Welke stoffen passeren moeder en embryo?
- Wat is bestuiving en bemesting?
- Wat is de functie en het gebruik van stikstof in uw lichaam?
- Is meer beter? Hoeveelheden en frequentie van kunstmelk aan kalveren onder hittestress
- Is de structuur in eukaryotische cellen die celactiviteiten regelt en genetisch materiaal bevat?
- Plantaardige eiwitten vervangen op aardolie gebaseerde grondstoffen

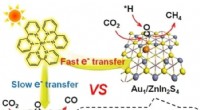
- Enkele goudatomen katalyseren de selectieve methanisering van kooldioxide
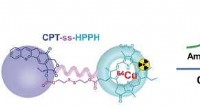
- Nanodeeltjes met multifunctionele medicijnprecursor voor synergetische tumortherapie
- De wetenschap achter perfecte aardappelen:vermijd lijmachtige textuur met precisie

- Van lint tot scroll:vormcontrole verkrijgen door elektrostatica

 Wat vertegenwoordigen contourlijnen op een topografische kaart?
Wat vertegenwoordigen contourlijnen op een topografische kaart?  Is ionisatie een exotherm of endotherm proces?
Is ionisatie een exotherm of endotherm proces?  Wat heeft fruitvliegstudies van het voor gen aangetoond?
Wat heeft fruitvliegstudies van het voor gen aangetoond?  Waar ligt de neritische zone van de oceaan?
Waar ligt de neritische zone van de oceaan?  Abiogenese biogenese vergelijken en contrasteren?
Abiogenese biogenese vergelijken en contrasteren?  Waarom is de zeer minder hoeveelheid warmte -energie geproduceerd in de verbindingsdraden?
Waarom is de zeer minder hoeveelheid warmte -energie geproduceerd in de verbindingsdraden?  Nieuwe studie illustreert de impact van de COVID-19-pandemie op werknemers en vakbondsleden in New York City
Nieuwe studie illustreert de impact van de COVID-19-pandemie op werknemers en vakbondsleden in New York City Welke rol speelt het milieu natuurlijke selectie?
Welke rol speelt het milieu natuurlijke selectie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

