
Wetenschap
Nanodeeltjes met multifunctionele medicijnprecursor voor synergetische tumortherapie
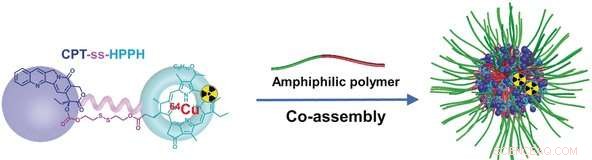
Krediet:Wiley
Voor een efficiënte kankertherapie met weinig bijwerkingen, het actieve geneesmiddel moet selectief een hoge concentratie in de tumor bereiken. In het journaal Angewandte Chemie , wetenschappers hebben een nieuwe benadering geïntroduceerd, waarin twee synergetische geneesmiddelcomponenten worden gecombineerd tot een dimeer. Dit dimeer kan in uitzonderlijk hoge concentraties worden opgenomen in polymere nanotransporters. De componenten worden geactiveerd wanneer het dimeer in de tumor wordt gesplitst. In aanvulling, ze maken het gebruik van twee verschillende beeldvormingstechnieken mogelijk.
Polymere micellen zijn de belangrijkste nanotransporters die worden gebruikt bij de behandeling van tumoren. Ondanks verbeterde transportsystemen, veel uitdagingen moeten nog worden overwonnen:onvoldoende laden, voortijdige afgifte van het medicijn, geen mogelijkheid om de distributie van het medicijn te controleren, en beperkte accumulatie van het geneesmiddel in het tumorweefsel. Longjiang Zhang, Guizhi Zhu, Xiaoyuan Chen, en hun team hebben deze problemen vanuit de andere richting benaderd. In plaats van de transporteur te verbeteren, ze verbeterden de lading.
De wetenschappers van de National Institutes of Health in Bethesda, VS, en Nanjing Universiteit, China, hebben een eenvoudige maar effectieve truc gebruikt:ze hebben twee medicijnen met elkaar verbonden, camptothecin en een speciale fotosensitizer, een dimeer maken. Micellen kunnen zeer efficiënt worden geladen met een ongewoon grote hoeveelheid van de dimere vracht (59%). De dimeren zijn minder hydrofiel dan hun individuele componenten, waardoor ze gemakkelijker kunnen worden ingebracht in het hydrofobe binnenste van de micellen. Om dezelfde reden, de dimeren verlaten de micellen niet terwijl ze door de bloedvaten reizen. Dit vermindert ongewenste bijwerkingen.
Beide componenten van het aanvankelijk inactieve dimeer zijn verbonden door een disulfidebrug die alleen kan worden verbroken door een glutathionafhankelijke reactiecascade. Glutathion is een klein eiwit dat in veel tumoren in hoge concentraties aanwezig is. Beide medicijnen worden pas geactiveerd nadat het dimeer in de tumorcellen is gesplitst.
Wanneer het gebied van de tumor wordt bestraald met laserlicht, de fotosensitizer zet normale zuurstof om in zeer reactieve singletzuurstof, die de cel beschadigt en een zuurstoftekort veroorzaakt. Camptothecine remt factor 1α, die cellen helpt om zuurstoftekort te weerstaan. Dit versterkt het cytotoxische effect van de fotosensibilisator. Een ander effect van camptothecine is dat het het DNA van de tumorcellen beschadigt.
In aanvulling, de fotosensitizer is een fluorescerende kleurstof en kan de radio-isotoop koper-64 binden, die visualisatie mogelijk maakt met zowel fluorescentiebeeldvorming als positronemissietomografie (PET). Kwantitatief PET zorgt voor nauwkeurige monitoring van het dimeer, evenals bevestiging van zijn farmacokinetiek en biodistributie in vivo.
Experimenten met celculturen en tumorachtige muizen toonden aan dat deze nieuwe methode het transport en de accumulatie van het medicijn in tumoren significant verbeterde met significant minder bijwerkingen, terwijl de tumor in een significant grotere mate krimpt dan toediening van de ongebonden individuele componenten.
 Onderzoekers presenteren inzichten in zoektocht naar nieuwe antibiotica
Onderzoekers presenteren inzichten in zoektocht naar nieuwe antibiotica Directe synthese van waterstofperoxide met behulp van TS-1-ondersteunde katalysatoren
Directe synthese van waterstofperoxide met behulp van TS-1-ondersteunde katalysatoren Wat is Variable Valency?
Wat is Variable Valency?
Elektronen bestaan in banen rond een atoomkern. Hoe hoger het aantal banen, hoe groter de afstand van de elektronen tot de kern. Atomen proberen een stabiele toestand te bereiken vergelijkbaar met die van de edelgassen of
 Hoe kristallen uit zout te maken
Hoe kristallen uit zout te maken  Verschil tussen natriumchloriet en natriumchloride
Verschil tussen natriumchloriet en natriumchloride
 Amazon dreigt te verbranden met dubbele brand, viruscrises
Amazon dreigt te verbranden met dubbele brand, viruscrises Nieuwe kennis van de aardmantel helpt de explosieve vulkanen van Indonesië te verklaren
Nieuwe kennis van de aardmantel helpt de explosieve vulkanen van Indonesië te verklaren Bewaarde pinguïnpoep onthult eerdere veranderingen in de circulatie in de Antarctische Oceaan
Bewaarde pinguïnpoep onthult eerdere veranderingen in de circulatie in de Antarctische Oceaan Niet genoeg fruit, groenten geteeld om de planeet te voeden, studie onthult
Niet genoeg fruit, groenten geteeld om de planeet te voeden, studie onthult Door het coronavirus veroorzaakte reducties in de uitstoot van kooldioxide zijn nog niet waarneembaar in de atmosfeer
Door het coronavirus veroorzaakte reducties in de uitstoot van kooldioxide zijn nog niet waarneembaar in de atmosfeer
Hoofdlijnen
- Zijn mensen echt afstammelingen van apen?
- Wat zijn lobben in een kern?
- Onderzoekers kijken naar de fruitvlieg om het menselijk brein te begrijpen
- Voordelen en nadelen van XRD en XRF
- Onderzoekers brengen dramatische achteruitgang in genetische diversiteit van noordwestelijke zalm in kaart
- De zoektocht naar de zuidelijke rubberboa
- Nieuwe gorilla in Audubon Zoo mag nog even binnen blijven
- Factoren die de primaire productiviteit beïnvloeden
- Kleine rode dieren schieten in het donker onder het ijs van een bevroren meer in Quebec
- Chemisch jongleren met drie deeltjes

- Onderzoekers lokaliseren de grootste celreceptor van het lichaam
- Loodvrij, efficiënte perovskiet voor fotovoltaïsche cellen
- Chemici leren een enzym een nieuwe truc, met potentieel voor het bouwen van nieuwe moleculen

- Formaatdehydrogenase reduceert koolstofdioxide tot mierenzuur
 Algemeen gebruik voor H2O
Algemeen gebruik voor H2O Chemisch bewijs laat zien hoe een dwergstelsel bijdraagt aan de groei van de Melkweg
Chemisch bewijs laat zien hoe een dwergstelsel bijdraagt aan de groei van de Melkweg Hoe overleven reuzenpanda's?
Hoe overleven reuzenpanda's?  Identiteit in online werelden begrijpen
Identiteit in online werelden begrijpen Hackers kunnen satellieten uitschakelen of ze in wapens veranderen
Hackers kunnen satellieten uitschakelen of ze in wapens veranderen Veel gasreuzen exoplaneten wachten om ontdekt te worden
Veel gasreuzen exoplaneten wachten om ontdekt te worden Nieuwe studie analyseert levensvatbaarheid van duurzame brandstoffen ontwikkeld via nieuw proces
Nieuwe studie analyseert levensvatbaarheid van duurzame brandstoffen ontwikkeld via nieuw proces Hoe maak je een raketauto met baking soda & azijn
Hoe maak je een raketauto met baking soda & azijn
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | German | Dutch | Danish | Norway | Swedish |

-
Wetenschap © https://nl.scienceaq.com

